锂电池产气行为分析
锂离子电池的产气行为是充放电循环、储存及滥用过程中,电极材料、电解液、界面膜及辅材发生副反应的核心外在表现,其气体组分(如H2、O2、CO₂、CO、C₂H₄、CH₄等)、产气速率及总量,直接关联电池的循环稳定性、体积膨胀率、安全性能及使用寿命。以下列举了大部分锂离子电池中气体的来源。
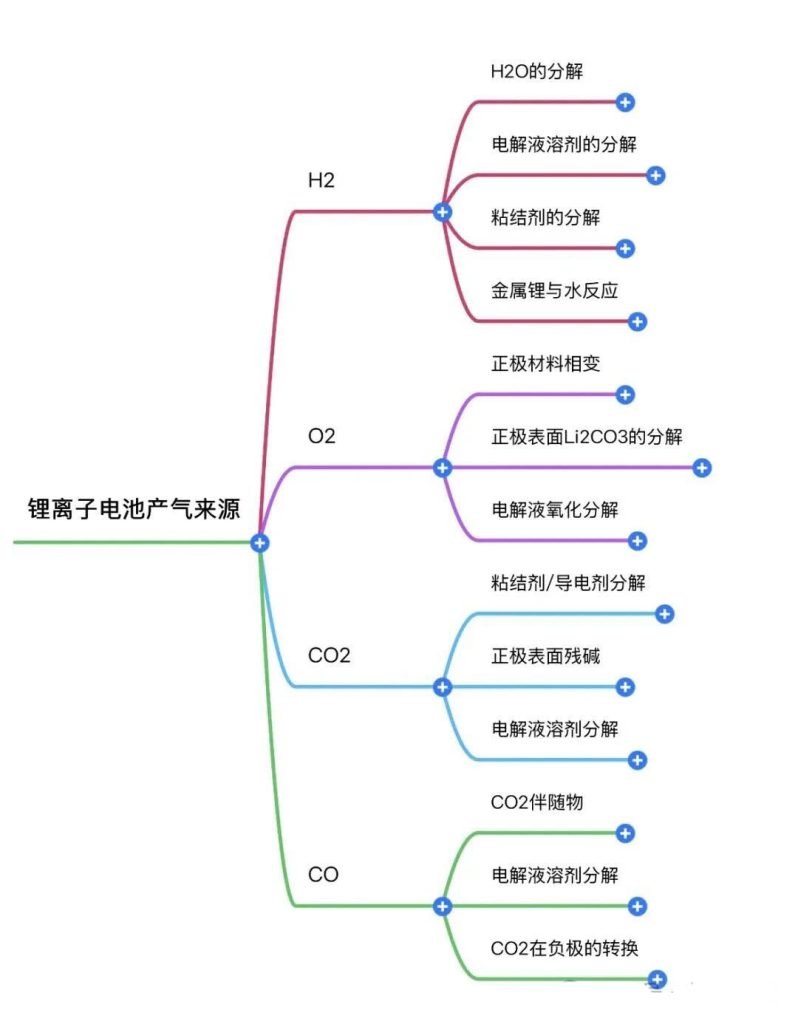
1.1H2的产生
H2作为电池产生的主要气体之一,主要来源于电池中水、电解液、黏结剂的分解以及锂与水的反应。
1.1.1 水的分解
由于电池内存在无法除尽的痕量水,当达到分解电势时,水分子在负极还原产生H2和OH-。这是氢气产生的基础途径,即使微量水分也可能在特定条件下引发氢气生成。
1.1.2 电解液中溶剂的分解
电解液中的溶剂在正极表面氧化失去电子转化为质子化的溶剂(记为R-H+),随后扩散至负极表面被还原,此过程需要正负极共同作用
1.1.3 黏结剂的分解
PVDF在高温或锂枝晶生长过程中可能发生分解,释放氢气:PVDF→分解产物+H2,是在锂枝晶与黏结剂接触时,氢气生成更为明显。
1.1.4锂与水反应
锂与水的反应当电池过充或内部短路导致锂金属析出时,锂与电池中的水分会发生剧烈反应:2Li+2H2O→2LiOH+H2此反应不仅产生氢气,还会释放大量热量,可能引发安全风险。
1.2 O2的产生
1.2.1 正极材料的相变
部分正极材料(如三元材料NCM、富锂锰基材料)在充放电过程中会发生结构相变,例如从层状结构转变为尖晶石相或岩盐相。相变过程中,晶格氧(O)从正极脱出,以单线态氧(¹O₂)等形式存在,随后通过与电解液溶剂的相互作用,转化为三线态氧(³O₂),即普通氧气(O₂)。这一过程与电池的充放电状态(SOC)密切相关,通常在高SOC(如80%以上)时更为显著。
1.2.2 正极表面Li2CO3的分解
NCM正极材料在制备过程中一般加入过量的LiOH以弥补锂盐在高温煅烧过程中的挥发损失,残余的锂在高温下以Li2O形式存在,冷却后接触到空气中的水和氧逐步转化LiOH和Li2CO3。这些正极表面残余的碱性物质以Li2CO3为主,在电池充电过程中分解产生O2。
1.2.3 电解液氧化分解
循环中后期氧气的重要补充来源,不是直接产氧,而是“间接释放氧元素”,本质是电解液被氧化拆解出氧:电解液溶剂(如EC、DMC、LiPF₆)被氧化断裂C-O键,拆解出的氧元素会:① 一部分结合成O₂释放;② 一部分和Li⁺结合生成Li₂O₂/Li₂O;③ 一部分参与生成CO₂、H₂O₂等副产物(伴随少量O₂);
1.3CO2的产生
CO2作为锂离子电池产气中最重要的成分,锂离子电池中CO₂的核心来源是含碳组分的氧化分解,包括导电炭黑的氧化以及正极表面残余Li2CO3和碳酸酯溶剂的分解。
1.3.1 负极/粘结剂/导电剂氧化分解
电池循环衰减后期或滥用时,辅材中的含碳组分被氧化,释放CO₂,是电池胀气加重的“推手”,也是热失控前期的信号之一:
1.3.2 正极表面残碱的分解及其与电解液间的反应
正极表面残余的LiOH碱性较强容易造成电解液分解产生CO2,Li2CO3则会在正极表面发生电化学氧化生成O2和CO2或与电解液中的HF反应生成LiF和CO2。
1.3.3 电解液中溶剂的氧化分解
1.4CO的产生
当作为氧化产物时,CO一般为CO2的伴随产物;当作为还原产物,一般为烯烃的伴随产物。此外,CO也可能是CO2在锂化石墨负极的转化产物。
1.4.1 CO2的伴随产物
导电炭黑以及电解液中溶剂分子被氧化生成CO2时往往伴随着CO,而且CO的量远低于CO2。
1.4.2 溶剂在负极的还原分解
CO是电解液含碳溶剂(EC/DMC/EMC等)在负极侧强还原环境下,碳链不完全断裂氧化的产物(完全氧化生成CO₂,不完全氧化生成CO),常规循环前期占比低,循环后期/硅基体系/异常工况下爆发式提升。
1.4.3 CO2在负极的转化
CO2在锂化石墨负极表面既会生成Li2C2O4,也会生成CO。
1.5 烯烃的产生
锂离子电池产气中的烯烃以乙烯(C₂H₄) 为主,少量伴随丙烯(C₃H₆),核心来源于电解液溶剂的还原分解,且与负极SEI膜的形成、破损修复直接强相关,常规工况下为首次化成阶段的特征产气,循环后期异常产气则对应界面稳定性失效。
1.6 烷烃的产生
锂电池产气中的烷烃以甲烷(CH₄)、乙烷(C₂H₆) 为主,少量丙烷(C₃H₈),核心来源于线性碳酸酯溶剂的还原分解(区别于环碳酸酯EC生成烯烃),同时与负极界面状态、电解液配比、循环工况强相关,常规工况下产气总量低于烯烃。
小结:锂电池产气机制尚存争议,如活性氧存在形式、电解液氧化限定条件等,需借助同位素标记、原位表征等先进技术深入探究。气体消耗转化与产生来源同等重要,电池内存在明显气串扰反应,仅依最终产气制定抑制策略效果有限。
