锂电池产气原理及基于电解液的抑制方案(一):H2,O2,烯烃,烷烃,CO2,CO
近年来与锂离子电池产气相关的报道主要聚焦于 H2、O2 、烯烃、烷烃、CO2和 CO等6类气体。本文则系统讨论这6类气体在锂离子电池使用过程中的产生机制以及这些气体的产生与电池性能变化之间的关系。由于电解液是锂电池产气的主要源头,且通过正负极材料改性提升电池稳定性和抑制产气的研究已有大量综述报道,本文基于电解液视角提出了一些相应的抑制策略。
1 锂离子电池中主要气体的产生机制
锂离子电池在生产(化成、分容)和使用过程中(充放电、存储)通常伴随着多类气体的产生,以下将逐一讨论这些气体的产生机制。
1.1 H2的产生
H2作为电池产生的主要气体之一,主要来源于电池中水、电解液以及黏结剂的分解。
1.1.1 水的分解
由于电池内存在无法除尽的痕量水,当达到分解电势时,水分子在负极还原产生H2和OH−。
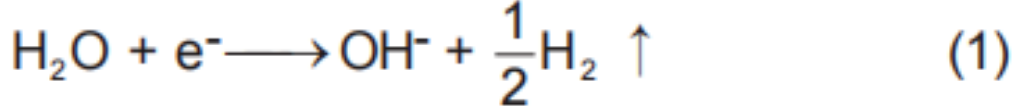
1.1.2 电解液中溶剂的分解
电池体系中引入的杂质水质量分数一般不高于0.01%,其分解产生H2的量也十分有限,然而在实际应用中,电池内检测到的H2含量却远高于水分解的理论值。Metzger等报道了H2的另一主要来源,即电解液中的溶剂在正极表面氧化失去电子转化为质子化的溶剂(记为 R-H+),随后扩散至负极表面被还原,此过程需要正负极共同作用,且与电池温度和电压相关[图1(a)、(b)]。Wang等则进一步发现该过程受到过渡金属的催化影响[图1(c)],3种过渡金属中Ni的催化活性最高,因而高镍正极材料体系导致了更严峻的产气。
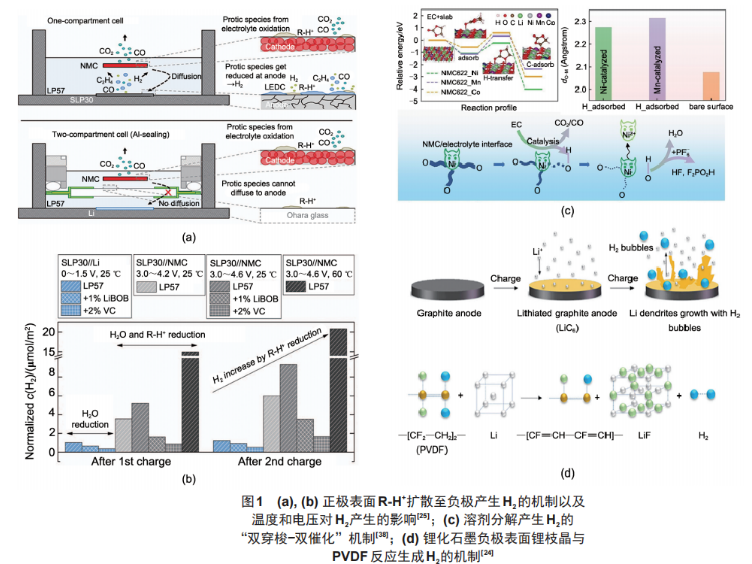
1.1.3 黏结剂的分解
Jin等采用原位光学显微镜观察了石墨电极表面锂枝晶的生长,此过程中伴随着大量H2气泡的产生,通过对比实验发现H2只产生在含有黏结剂PVDF的电极表面[图1(d)]。
1.2 O2的产生
O2作为锂离子电池中正极产生的气体,主要来源于正极材料的结构相变和表面残余Li2CO3的分解。
1.2.1 正极材料的相变
NCM在使用过程中存在着不可逆相转变过程,即由层状结构转变为尖晶石相最终转变为岩盐相并析出O2,与NCM具有类似结构的LCO同样存在不可逆相变问题,富锂锰基正极材料在高电压状态下,也会出现析氧问题。相变过程中晶格氧(lattice oxygen,[O])从正极脱出,其具体存在形式主要有氧自由基(·O或⋅O2−)和单线态氧(singlet oxygen,1O2)两种学说模型,以下以单线态氧模型为例(图2)。单线态1O2处于激发态,分子能量较高,其在电解液中有4种路径释放能量:①以电子振动耦合的形式将能量转移至溶剂分子转化为三线态氧(triplet oxygen,3O2),即空气中O2的存在形式;②与电解液中溶剂分子发生化学反应生成氧化物;③以磷光发射的形式转化为3O2,释放出波长为1270nm 的光;④两分子的1O2碰撞生成3O2,并释放出波长为633nm的光。4种方式中路径①占主导地位,这也是电池中O2的主要来源,其反应速率主要由溶剂的分子振动性能和介电常数决定。其次为路径②,此过程中伴随着其他气体的产生,只有少部分的1O2通过路径③、④转化为3O2。研究表明当电池状态达到80% SOC,1O2开始显著产生。
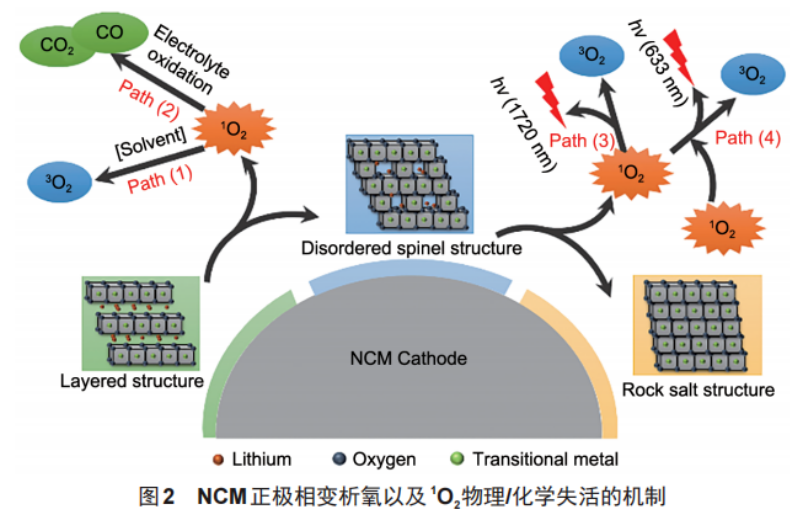
1.2.2 正极表面Li2CO3的分解
NCM正极材料在制备过程中一般加入过量的LiOH以弥补锂盐在高温煅烧过程中的挥发损失,残余的锂在高温下以Li2O形式存在,冷却后接触到空气中的水和氧逐步转化LiOH和Li2CO3。这些正极表面残余的碱性物质以Li2CO3为主,在电池充电过程中分解产生O2[式(2)]。
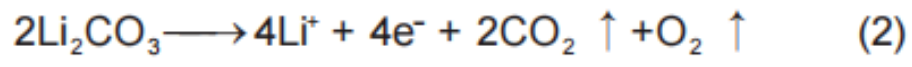
1.3 烯烃的产生
锂电池产气的烯烃主要为C2H4,来源于电解液中碳酸乙烯酯(EC)的还原分解,此过程通常伴随着SEI的形成与修复。路径Ⅰ为经典的EC单电子还原过程(图3),生成LiO2COCH2CH2OCO2Li(LEDC)和C2H4[式(3)]。
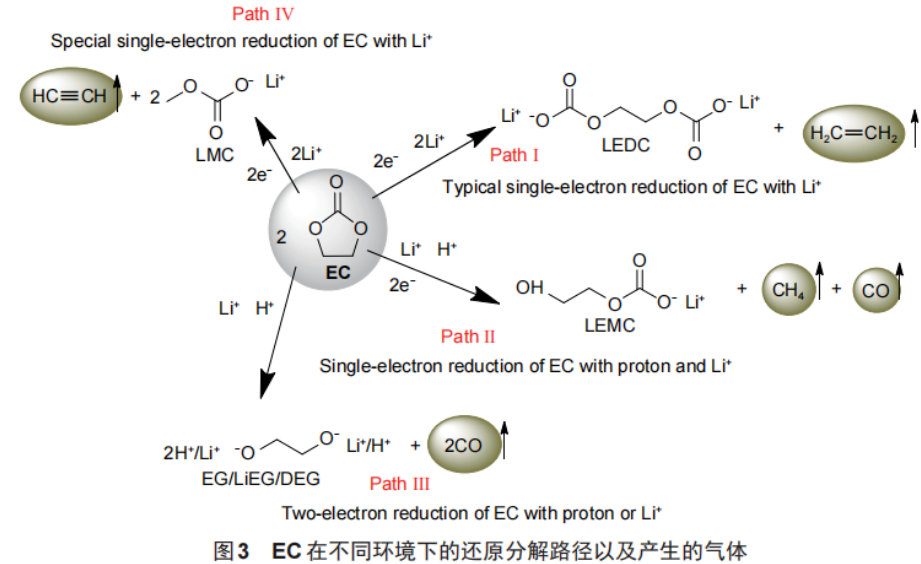
因此在电池制作工艺中,化成产气后会进一步抽除电池内部的气体然后再进行二次封装。如果化成阶段产生的SEI稳定性较差,电池将在后续的使用中继续发生电解液分解产生C2H4。同理电池内C3H6的产生则主要来源于碳酸丙烯酯(PC)的分解。

1.4 烷烃的产生
锂电池产气中的烷烃主要为CH4和C2H6,来源于线性碳酸酯在负极发生的还原分解,其中CH4主要来源于含有甲基的线性碳酸酯,如碳酸二甲酯(DMC),C2H6则来源于碳酸二乙酯(DEC),碳酸甲乙酯(EMC)分解则会同时产生CH4和C2H6。当从A处断键时,DEC发生单电子还原并与质子结合生成C2H6;当从B处断键,DEC发生双电子还原生成CO(图4)。
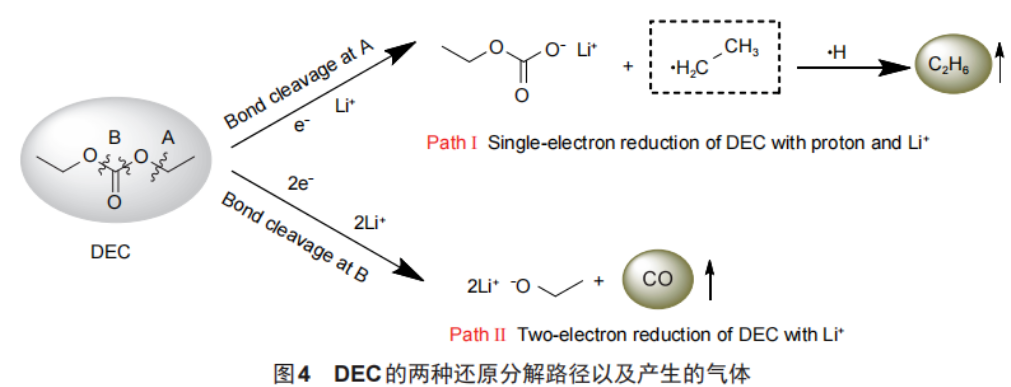
然而在实际测试中多次在EC/DEC体系电池产气中检测到了CH4的存在,Teng等也报道了这一现象,说明CH4除了来源于含甲基的线性碳酸酯外,还有可能来源于环状碳酸酯EC[式(4)]。

1.5 CO2的产生
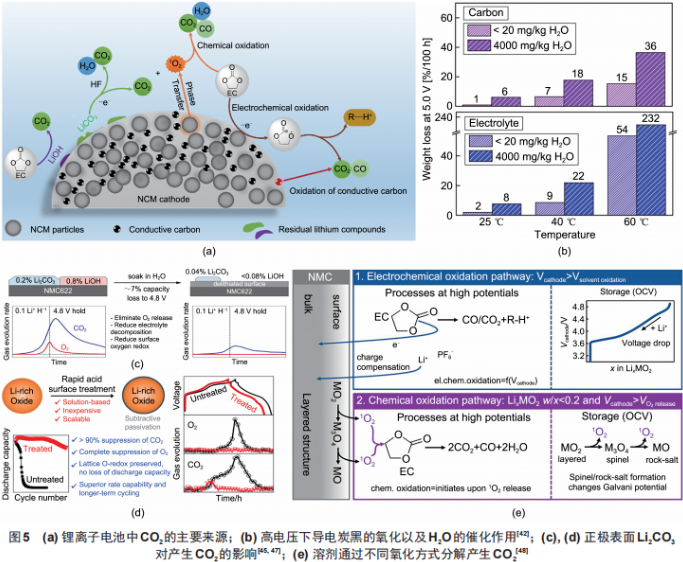
CO2作为锂离子电池产气中最重要的成分,来源于导电炭黑的氧化以及正极表面残余Li2CO3和碳酸酯溶剂的分解[图5(a)]。
1.5.1 导电炭黑的氧化
导电炭黑的氧化产物是CO和CO2的混合气体,其中CO2的含量大约为CO的6倍。当电池处于60℃以及5.0V的上限电压下,约有质量分数15%的导电炭黑会被氧化,而当有水存在时,氧化进一步加剧[图5(b)],这也表明了高电压体系不仅对电极材料有更高的要求,对导电炭黑的稳定性也会是一个巨大的挑战。
1.5.2 正极表面残碱的分解及其与电解液间的反应
正极表面残余的LiOH碱性较强容易造成电解液分解产生CO2,Li2CO3则会在正极表面发生电化学氧化生成1O2和CO2[式(2)]或与电解液中的HF反应生成LiF和CO2[式(5)]。
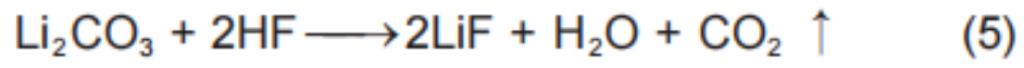
McCloskey等认为在锂离子电池首次充电中,CO2和CO主要来源于Li2CO3的分解而非电解液,将正极表面进行酸处理后,CO2/CO也随之成比例减少。将酸替换为温和的水或甲醇溶剂,同样可以减少CO2/CO的产生[图5(c)]。这种对正极表面进行溶剂清洗的方法不仅可以降低CO2/CO的产生,还可以抑制O2的产生[图5(d)]。
1.5.3 电解液中溶剂的氧化分解
溶剂的氧化分解是电池中CO2的最主要来源,溶剂直接在正极表面失去电子生成CO2被称为电化学氧化,被[O]氧化生成CO2则称为化学氧化[图5(e)]。
何种氧化方式占主导作用一直是学者研究讨论的热点。传统观念认为电解液中溶剂分子的氧化主要发生在正极材料表面,属于电催化过程,因而气体产生的速率主要由正极材料的催化活性、比表面积以及电压窗口所决定。然而近年来随着原位差分电化学质谱(DEMS)等表征方法的发展,更多证据表明电解液的氧化分解方式主要为化学氧化,因为CO2和CO气体的产生总是伴随着[O]和O2的出现,而且电解液中溶剂氧化产生CO2由电池SOC决定而非正极电势。
1.6 CO的产生
当作为氧化产物时,CO一般为CO2的伴随产物;当作为还原产物,一般为烯烃的伴随产物。此外,CO也可能是CO2在锂化石墨负极的转化产物。
1.6.1 CO2的伴随产物
导电炭黑以及电解液中溶剂分子被氧化生成CO2时往往伴随着CO,而且CO的量远低于CO2。
1.6.2 EC在负极的还原分解
EC在负极的分解路径除了经典的单电子还原模型(图3,路径I),还有双电子还原模型(图3,路径Ⅲ),该过程产生的气体均为CO。另一方面,当EC按照路径Ⅲ分解产生CH4时也伴随着CO的产生。目前关于EC在负极分解的主流观点为路径I,这主要因为路径Ⅱ、Ⅲ中需要假定H+的存在,而电解液溶剂一般为质子惰性的碳酸酯。然而事实上,250μL电解液中10mg/kg的H2O会产生约280nmol的H+,这已远大于路径Ⅱ中所需H+的量(约20nmol)。
1.6.3 CO2在负极的转化
Ellis等通过XPS表征发现CO2在锂化石墨负极表面既会生成Li2C2O4[式(6)],也会生成CO[式(7)]。
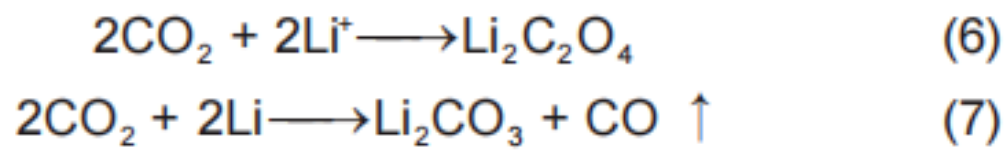
1.7气体在正负极间的串扰反应
锂电池内产生的气体并非稳定存在,其可能在正负极间穿梭发生串扰反应。Liu等发现NCM正极释放的活性氧可以扩散至负极与锂化石墨反应释放大量热量,使得电池在未发生短路时便可积聚热量触发热失控[图6(a)]。Wang等发现负极产生的还原性气体同样可以扩散至正极表面诱发NCM正极相变析氧,随后发生化学反应生成CO2和H2O,并释放大量热量引发热失控[图6(b)]。
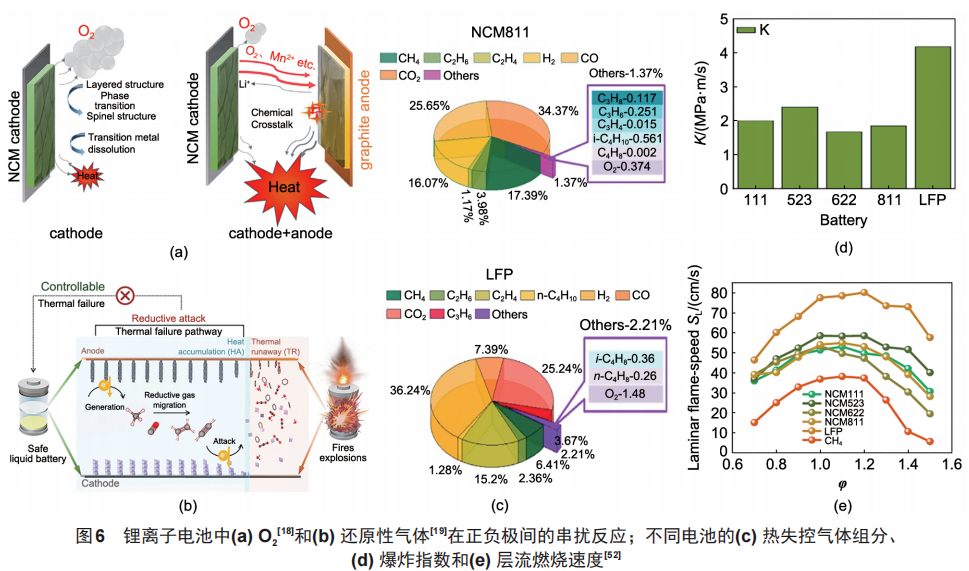
这些串扰反应及其引发的热失控均与正极析出的活性氧相关,因而理论上NCM电池相对于LFP电池具有更高的危险性。事实上,LFP相对于NCM确实具有更高的热失控引发温度、更低的热失控最高温度以及更少的产气量,因而更适用于储能电站。然而新的研究表明,由于缺少正极材料的析氧作用,LFP电池在过充条件下相对于NCM电
池会产生更多的H2、C2H4等还原性气体[图6(c)],使得LFP电池具有更低的爆炸极限以及更高的爆炸压力和爆炸指数[图6(d)、(e)]。此外,H2、C2H4比例的提高使得LFP电池的热失控气体具有更高的层流燃烧速度,因而火焰传播速度更快,极大增加
了储能电站的风险等级。由于H2相对于其他挥发性气体以及烟感报警器具有更高的灵敏度、更早的预警时间和更明显的变化特征,因而通过对H2进行监测,随后进行外界干扰降低H2、C2H4等还原性气体的浓度可以有效减少储能电站的安全事故。
