锂电池Ni-Co-Mn基正极材料前驱体的形核调控及机制(一)
三元正极材料LiNixCoyMn1−x−yO2具有较高的理论容量和超过220mAh/g的实际容量。其中Ni元素具有较宽的氧化还原范围(+2/+3/+4),成为氧化还原反应主要活性离子;Co3+的eg和t2g轨道不含未成对电子,可部分消除Ni2+/Ni3+与Mn4+之间的磁阻滞,避免与Ni2+发生180°超交换作用,抑制锂镍混排,提升锂离子传输动力学;Mn在充放电过程中维持+4价,稳定脱锂后材料晶体结构,提高热稳定性,因此在制备过程中实现Ni、Co、Mn均匀混合,减少元素偏析成为三元正极材料性能发挥的前提。
实验室和工业生产中常采用共沉淀法制备三元材料前驱体NixCoyMn1−x−y(OH)2,之后加入锂盐烧结得到三元正极材料。该方法批次性强,产量大,可通过调整共沉淀反应参数定向调控前驱体材料粒径大小、晶粒形貌以及致密度,满足不同应用场景的三元正极材料制备需求。
三元正极材料晶体结构为前驱体晶体结构的拓扑转变,前驱体材料的结晶性、晶粒形态、粒径以及球形度等理化性能直接决定了三元正极材料的性能发挥。然而,前驱体生长过程对于共沉淀反应环境变化极为敏感,不同化学成分乃至同一化学成分不同粒径前驱体生长参数存在较大差异,易获得结晶性差、球形度差、疏松多孔前驱体。如何在保证三种元素均匀共沉淀的基础上,调节十余种反应参数,获得理想目标产物,成为共沉淀反应过程难点所在。
本文以共沉淀法制备三元正极材料前驱体为主体内容,首先阐述共沉淀基础理论,包括置换沉淀反应实现元素共沉淀,及通过沉淀物过饱和度调控前驱体形核方式与速率基本原理。接着从晶面择优生长角度,结合溶解-再结晶过程解释了片状、棒状一次颗粒和球形二次颗粒团聚体的生长过程。最后基本涵盖了共沉淀反应过程中所有可变参数,包括反应体系pH值、总氨浓度、固含量、反应时间、反应温度、底液体积比、搅拌速度、反应釜结构、陈化时间以及反应气氛及烘干气氛,深入讨论了每种反应参数由低到高变化对共沉淀反应形核热力学及动力学的影响,最终得到不同理化性能的前驱体材料。
2 Ni-Co-Mn基正极材料前驱体形核理论与影响因素
将原料溶于溶剂中得到混合溶液,之后加入合适的沉淀剂和络合剂,使溶液中的原料同时沉淀,称为共沉淀法。三元材料共沉淀法又可分为直接共沉淀法和间接共沉淀法。直接共沉淀法将锂盐、镍盐、钴盐、锰盐混合溶解,之后加入沉淀剂和络合剂使四种盐同时沉淀,经过热处理得到三元材料。直接共沉淀法一步沉淀,过程简单,但
由于锂盐和过渡金属盐溶度积差异较大,使得同时沉淀难度较大。更常见的为间接共沉淀法,即通过合适浓度的沉淀剂和络合剂,使得符合化学计量比的混合盐溶液同时沉淀,得到三元材料前驱体,之后加入锂盐高温烧结制备具有一定形貌的三元正极材料。
间接共沉淀法获得的前驱体一般为亚微米级一次颗粒团聚而成的微米级球形二次颗粒,如图1b、c所示,每个亚微米级一次颗粒为一个单晶,这种特殊的球形形貌在后续烧结过程中,排列相近的一次颗粒发生重熔或崩解,获得多晶球状或单晶颗粒状三元正极材料,满足不同使用需求。
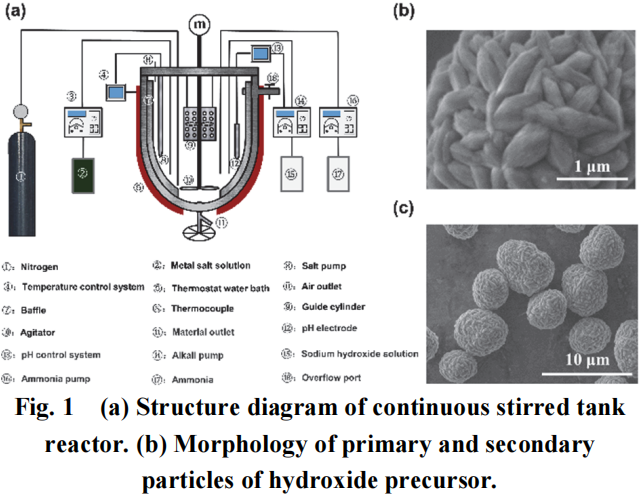
共沉淀反应在反应釜中进行,图1a为共沉淀反应釜设备示意图,沉淀剂、络合剂(助剂)和混合盐溶液分别加入三个储料罐中,通过蠕动泵软管连接至反应釜进料口,助剂泵和盐泵转速可人为设定,碱泵转速由在线pH控制系统通过探入反应釜内的在线pH电极反馈的信号进行比例积分微分算法(PID程序)控制,以维持恒定的pH环境。反应釜采用恒温水浴加热,加热系统对热电偶反馈的温度信号进行PID程序控制,以获得恒定的温度。反应釜内安装多级搅拌系统、导流筒、挡流板等,设置进气口和排气口,预留部分备用阀满足后续加装需求,设置出料口和溢流口实现浓缩工艺。一些大型反应釜还会设置独立浓缩釜、陈化釜等,不同功能釜相互串联连接及时分离产品,提高生产效率。
2.1 共沉淀法制备前驱体基础理论
在实际生产过程中,除了盐溶液和沉淀剂,还需要添加络合剂(也称为助剂,一般为氨水)使离子与沉淀剂的直接沉淀反应,转换成离子与氨分子络合,再与沉淀剂发生置换沉淀反应,从而实现Ni2+、Co2+和Mn2+均匀共沉淀,同时减缓沉淀速率使沉淀反应更可控。下面将从溶度积角度分析络合剂在实现元素共沉淀及控制沉淀速率方面起到的关键作用,及阐述通过调控沉淀物的绝对过饱和度引发不同形核模式,改变前驱体生长过程的基本原理,这一原理将贯穿前驱体共沉淀过程影响因素内容部分。
2.1.1 络合置换反应调控前驱体共沉淀速率基本原理
难溶电解质AnBm在特定溶剂中达到溶解平衡时,存在以下溶解平衡反应:
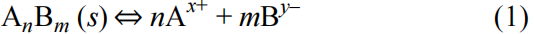
反应达到平衡状态后,在一定温度下,难溶电解质饱和溶液中,各离子活度化学系数次幂的乘积为一常数,称为溶度积常数,简称溶度积,用Ksp表示。在稀溶液中,也可用离子浓度代替活度。

溶度积与物质的本性和温度有关,而与离子浓度的改变无关,反映难溶电解质在溶液中生成沉淀的难易程度。在温度298 K时,三元材料所含元素的沉淀平衡反应及对应的Ksp’ 如下:
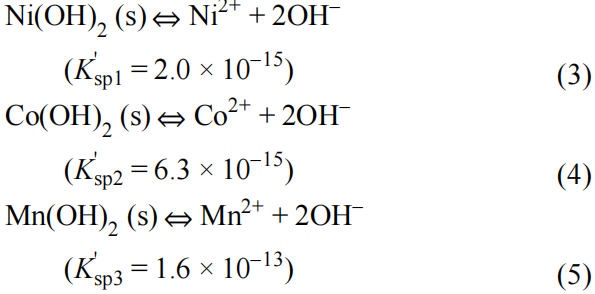
只有沉淀剂OH−存在的情况下,三种元素的溶度积较小,会使得三种沉淀反应的离子积大于溶度积,使沉淀平衡反应向生成沉淀方向移动,造成爆发式形核,形核速率不可控。同时由于Mn2+沉淀平衡反应的溶度积比Ni2+和Co2+的大两个数量级,造成Ni2+和Co2+优先沉淀,使得元素分离无法实现三种元素均匀共沉淀。当加入氨水作为络合剂后,NH3先与游离的过渡金属离子发生络合反应生成络合物,并存在以下络合平衡反应:
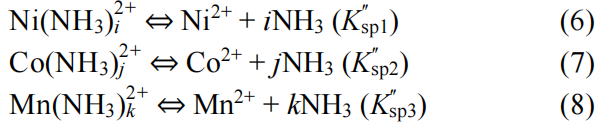
之后在沉淀剂的作用下,发生置换沉淀反应,释放出NH3同时生成Ni(OH)2(s)、Co(OH)2(s)以及Mn(OH)2(s),如下式所示:
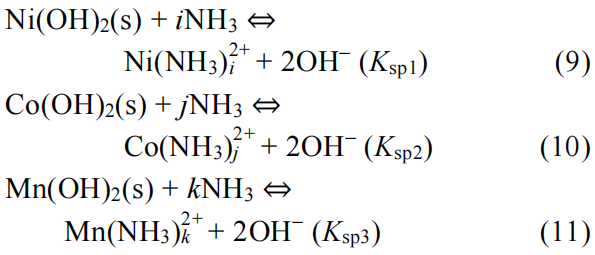
例如:当i = j= k=1时,式(6)、(7)、(8)可具体为:
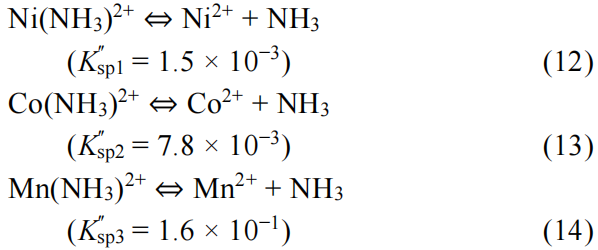
则置换沉淀反应可具体为:
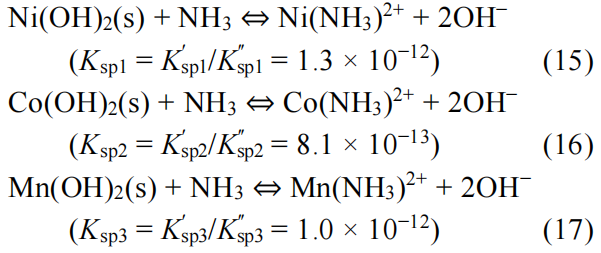
当加入氨水作为络合剂后,三种元素的置换沉淀平衡反应溶度积同时变大,且基本相同,这有利于减缓沉淀速率使沉淀反应更加可控,同时实现三种元素均匀共沉淀。
2.1.2 前驱体形核方式与速率调控原理
形核方式可以分为均匀形核与非均匀形核。均匀形核是指晶核由液相中的一些原子团直接形成,不受杂质粒子和外表面的影响。非均匀形核也称为异质形核,是指新相优先在液相中存在的异质处形核,即依附于液相中的杂质或外来表面形核。在共沉淀反应过程中,反应初期以均匀形核为主以增加活性位点,随反应时间延长在原有晶核表面非均匀形核,可见非均匀形核的基本原理建立在均匀形核基础上,因此先讨论均匀形核过程而后过渡至非均匀形核。
在沉淀剂和络合剂的作用下,式(9)、(10)、(11)所示置换沉淀平衡反应被打破,向生成沉淀方向移动,此时离子之间相互碰撞形成离子集团,离子集团呈现局部有序排列,很可能成为均匀形核的晶核。当出现晶核后,离子由液相中的混乱状态转变为有序排列的晶态,体系内体积自由能的降低为形核驱动力,另一方面晶核会形成新的表面,引起的表面自由能的增加为形核阻力,晶核形成时体积应变能在液相环境中可被释放。假定晶核为球形,如图2a所示,半径为r,ΔGV为单位体积晶核出现时体积自由能的降低值,σ为固液界面比表面能,可用表面张力表示。当溶液中出现第一个晶核时,总的自由能变化可表示为:
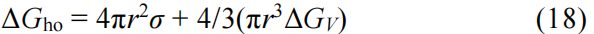
在一定温度下,体系总自由能ΔGho是r的函数,关系曲线如图2c所示,ΔGho在半径为r*时达到最大值,当晶核半径r<r*时,晶核长大将导致体系总自由能增加,因此这种尺寸晶核不稳定,最终反溶于液相中,当r≥r*时,晶核长大使得体系总自由能降低,此时晶核可以稳定存在,故称r*为晶核的临界半径,只有超越这一尺寸的晶核才能在液相环境中稳定存在。
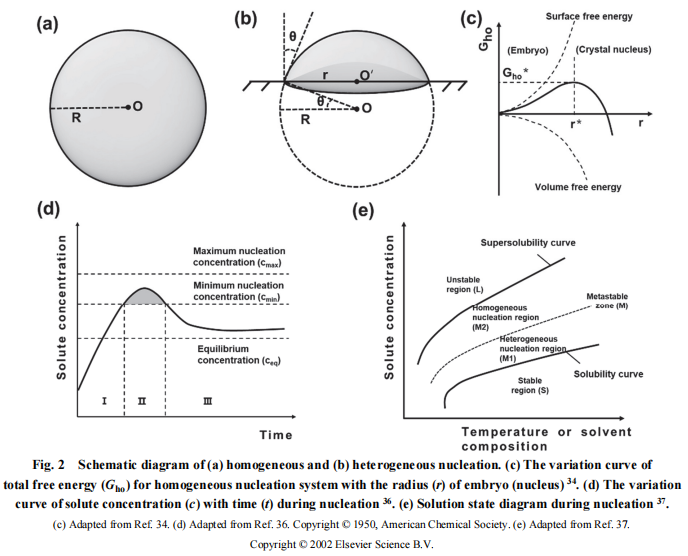
当溶液体系存在晶核或杂质颗粒时,后续出现的晶核就会依附于原有晶核表面,此时晶核为被平面所截的球冠,相关示意图如图2b,θ为晶核边缘切线方向与垂直方向的夹角,夹角范围为0°–90°。此时出现第一个球冠晶核时,总自由能的变化可表示为:
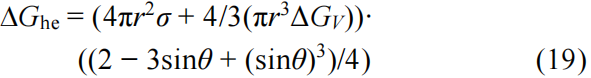
可以得出,非均匀形核总自由能的变化值恒小于均匀形核,即在溶液体系已有晶核的条件下,此时更倾向于依附于已有晶核表面形核。
溶质实时浓度c与溶质平衡浓度ceq之间的差值称为绝对过饱和度,以下统称过饱和度。在溶液体系内,只有当溶质的浓度c高于平衡浓度ceq时,才可以析出结晶物。图2d展示了形核过程中溶液溶质浓度随时间的变化关系,当溶质浓度c介于平衡浓度ceq和最低形核浓度cmin之间时,此时没有晶核产生,但加入晶核后可以依附于晶核析出结晶物(非均匀形核)。当溶质浓度介于最低形核浓度cmin和最高形核浓度cmax之间时,即区域II,同时发生均匀形核与非均匀形核过程。
随着溶质被消耗,溶质浓度达到最大值后开始降低,进入区域III后,均匀形核过程结束,晶核进入非均匀形核生长阶段,直到溶质浓度低于平衡浓度ceq,生长过程结束。可以发现非均匀形核的起始溶质浓度为平衡浓度ceq,而均匀形核的起始浓度为最低形核浓度cmin,与上述关于形核方式的讨论结果保持一致。在不同温度和溶剂组成条件下,按照溶质浓度将溶液分为稳定态、介稳态和不稳定态,如图2e所示,当c<ceq时,此时为不饱和溶液,处于稳定态S区。
当溶质浓度位于M区时,可进一步细分为M1区和M2区,M1区为养晶区,对应图2d中ceq≤c<cmin,此时为低过饱和溶液,不会发生均匀形核过程,但加入晶核后可以依附晶核发生非均匀形核过程。当进入M2区后,达到均匀形核条件,可在溶液体系中自发形核,对应cmin≤c<cmax。伴随溶质浓度升高进入不稳定态L区,此时发生爆发式形核,形核生长速率难以控制。当对前驱体粒径分布有特殊要求时,可向反应体系加入预制晶核,调整反应参数将沉淀物浓度控制在M1养晶区,在晶核表面定向生长获得粒径分布集中的前驱体。
当式(9)至(11)所示的置换沉淀反应平衡向生成沉淀方向进行速率较快时,沉淀物过饱和度较高,可独立形核,也称为均匀形核。当生成沉淀速率较慢或向沉淀溶解方向进行时,沉淀物过饱和度较低,此时倾向于依附原有晶核表面形核,称为非均匀形核,即生长过程。沉淀剂和络合剂以及其余共沉淀反应参数作用的本质是调节置换沉淀反应平衡移动方向,控制沉淀物的生成速率,调节沉淀物的过饱和度,使之达到不同形核方式主导的反应条件。在反应釜加料初期,溶质浓度开始提升,由于体系不存在晶核将跨越养晶区进入均匀形核区,均匀形核和非均匀形核同时发生,此时固液比小,晶核数量少,有效活性位点少,这使得一次颗粒尺寸小,生长缓慢,此时体系以均匀形核为主增加活性位点,同时为了降低表面能,一次颗粒快速凝并团聚为二次颗粒,二次颗粒再次凝并堆积导致结构疏松,内部空隙多,球形度差;不断加料过程中固含量上升,由于液相占比降低提升了沉淀物过饱和度,进一步促进均匀形核的发生,晶核停止凝并生长并独立存在于液相环境中,晶核数量增多使得生长活性位点增多,同时存在的非均匀形核过程促使一次颗粒尺寸和二次颗粒粒径增加;通过调节反应参数降低沉淀物过饱和度后,进入养晶区,此时依据体系内存在的晶核主要发生非均匀形核过程,二次颗粒表面沟壑和内部空隙得到填充,但暴露的生长位点越来越少;在反应后期进入慢速生长阶段,一部分晶核由于不能找到合适的生长位点,独立团聚成为新的一次颗粒,凝并生长引发二次形核,拓宽粒度分布跨度,出现大颗粒夹杂小颗粒的微观形貌。以上是从共沉淀反应整个过程出发,结合沉淀物过饱和度和活性位点变化以及能量最低原理解释前驱体的形核生长过程,下一节将由晶体结构出发,从晶面择优生长角度详细讨论一次颗粒和二次颗粒的形核生长过程。
