用模拟验证电池电化学测试的适用性
锂离子电池电极过程包括:①溶剂化的锂离子从电解液内迁移到电解液/固体电极的两相界面;②溶剂化的锂离子吸附在电解液/固体电极的两相界面;③去溶剂化;④电荷转移,电子注入电极材料的导带,吸附态的锂离子从电解液相迁移至活性材料表面晶格;⑤锂离子从活性材料表面晶格向内部扩散或迁移;⑥电子从集流体向活性材料的迁移。这些过程可以用经典的P2D模型来描述,在模型中:步骤①和⑤分别对应电解液和固相颗粒内部的离子扩散,由菲克定律描述,是造成浓度极化的主因。核心的界面过程③和④,即去溶剂化与电荷转移,被整合为Butler-Volmer动力学方程来描述,其反应速率强烈依赖于界面处的锂离子浓度和固相颗粒表面的电势,这直接决定了电化学极化的程度。步骤⑥的电子迁移,由于电极材料导电性好,通常简化为欧姆定律。

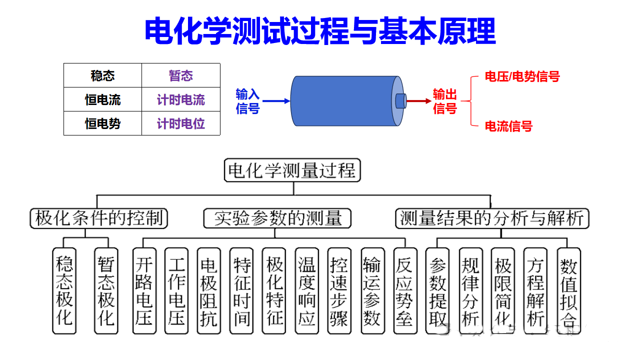
电化学测试是研究锂离子电池系统的最常见方法。电化学测试的底层逻辑源于对电化学体系施加一个可控的“输入信号”并监测其“输出信号”,通过分析这种刺激-响应关系来解析体系内部的内在规律。整个测试过程始于对极化条件的精确控制,其核心范式分为稳态与暂态两大类:稳态测试(如恒电流、恒电势)通过观察系统达到平衡后的状态来揭示其宏观的极化特征与控速步骤;而暂态测试(如计时电流、计时电位)则通过施加快速扰动并监测动态响应,利用体系达到稳态前的弛豫过程来解析电极阻抗、特征时间等动力学参数。
举三个常见的电化学测试例子:CV、EIS和GITT。循环伏安(CV)通过控制电极电势以三角波形循环扫描,并同步测量响应电流,从而在电势-电流图中呈现一对或多个氧化还原电流峰,主要用于定性分析电极上可逆反应的发生电位、反应机理及副反应。电化学阻抗谱(EIS)则向电化学体系施加一个不同频率的小幅正弦电势扰动,并测量其电流响应以计算阻抗,通过分析阻抗随频率的变化(奈奎斯特图或波特图),能够解析电极过程中不同时间尺度的动力学步骤(如电荷转移、离子扩散、表面膜电阻等)及其耦合关系。而恒电流间歇滴定技术(GITT)结合了暂态与稳态测量,它对待测体系施加一个短时间的恒电流脉冲,随后是一个长时间的静置弛豫以恢复平衡,通过分析脉冲期间的暂态电势变化和弛豫后的稳态电势偏移,可以定量计算锂离子在电极材料中的扩散系数,并准确关联电极组成与平衡电势。
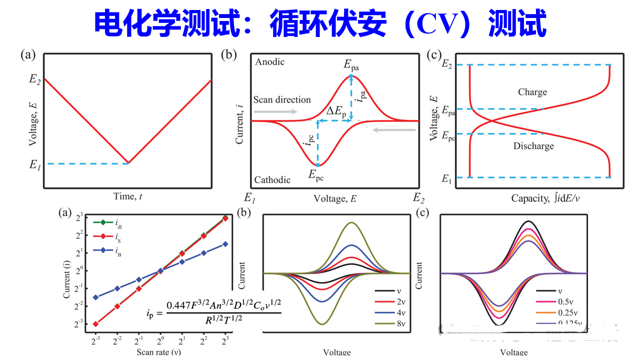
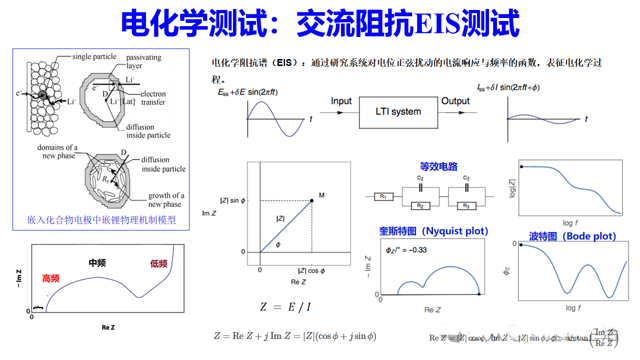
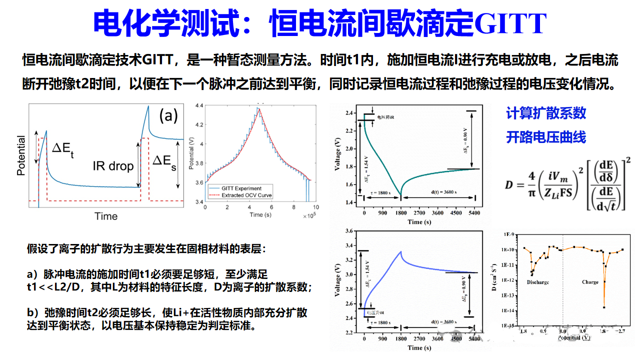
但是,这些电化学测试方法往往都有前提条件或者数据分析很难。比如根据CV峰值电流计算扩散系数要求电极反应必须是完全可逆的,整个电极过程的速率控制步骤必须是扩散步骤。而EIS数据分析等效电路的选择非常关键,常常伴随主观随意性比较大,导致分析错误。因此,接下来一段时间,我计划采用comsol有限元模拟的方法研究电化学测试的适用性。
首先,根据建立P2D锂离子电池模型,明确定义电极反应动力学参数(交换电流密度、传递系数)与物质传输属性(扩散系数、迁移率)等参数,系统性地引入可控变量(如电荷转移速率、扩散速率、双电层电容、溶液电阻),模拟不同极化条件下(从可逆到完全不可逆)的循环伏安曲线,以及从1 mHz到100 kHz频率范围的电化学阻抗谱;随后将模拟数据分别用Randles-Sevcik方程和预设等效电路(如Randles电路、Warburg扩散元件)进行反演分析,定量比较在不同动力学区域(混合控制、扩散控制、电荷转移控制)下传统方程与有限元结果的偏差。最终分析测试方法的适用性。
