扣式全电池设计 组装和测试教程与实例分析
1.前言
全电池是包含正极、负极、隔膜、电解液和壳体的完整电池系统。与半电池不同,全电池能够提供实际电池在工作时的电化学性能和机械性能的准确评估。半电池通常是以金属片或箔(如锂片或锂箔)作为对电极,而全电池则是由两个活性电极组成,一个作为正极,另一个作为负极。全电池的设计和组装需要考虑多种因素,包括电极材料的选择、电解液的类型、隔膜的属性以及电池壳体的结构等,以确保电池的性能、安全性和可靠性。全电池的测试通常用于评估正负极材料与电池其余部分的匹配程度,以及电池在实际使用条件下的性能表现。本文主要以实验室扣式全电池为基础,介绍全电池设计、组装和测试,并结合实例分析影响全电池设计的因素。
2.全电池概述
2.1 定义
全电池是指具备所有组件的完整电池系统,包括正极、负极、电解液、隔膜和外壳。它能够实际进行电能的存储与释放,是评估电池材料在实际工作条件下性能的重要工具。在全电池中,正极和负极材料通过氧化还原反应进行电能和化学能转换,电解液和隔膜则分别负责离子的迁移和防止两极直接接触造成短路
2.2 工作原理
全电池的工作原理基于正负极材料之间的氧化还原反应。以磷酸铁锂(LiFePO4)正极、石墨(C)负极为例,在充电时外界施加的电压使得LiFePO4中的Li+脱出并迁移到磷酸铁锂的表面,然后在外电压的持续作用下,进入电解液并穿过隔膜后再进入电解液中,继续迁移至石墨表面,最后嵌入到石墨中。而与此同时,电子作用于外部器件后快速到达石墨侧,使整个电池体系保持电荷平衡,从而实现充电过程的顺利进行。放电时Li+运动方向和电池发生的电化学反应与充电过程相反。扣式电池组成示意图如图1所示。
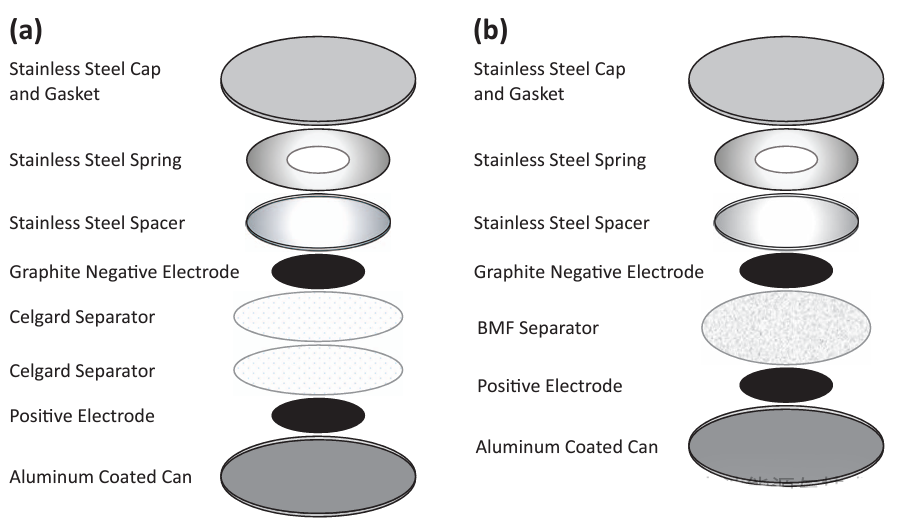
图1. 扣式电池各组分示意图
(a)两个Celgard隔膜和(b)一个聚丙烯吹塑微纤维(BMF)隔膜。(doi:10.1149/2.1171902jes)
3.全电池设计和组装
3.1 设计依据
扣式全电池设计依据主要考虑N/P比、Overhang和首次库伦效率(ICE)。下面将对上述依据进行介绍。
3.1.1 N/P比
1.定义:指在同一阶段和同一条件下,正对面的负极材料容量超过正极材料容量过量的比例,也称为CB值(Cell balance)。
[注]N/P比一般在1.05~1.20之间,负极过量是避免金属沉积导致枝晶产生,但从能量密度和生产成本方面考虑,负极过量又应该尽可能低。在实验室中,N/P比的设定通常较为灵活,保证组装的全电池能够稳定实现循环即可。
2. N/P比计算公式:N/P=(负极活性物质比容量×负极活性物质面密度×负极活性物质含量)/(正极活性物质比容量×正极活性物质面密度×负极活性物质含量)
[注释]N/P计算时,(1)同一阶段指由于电池存在充电过程和放电过程,对应着不同的比容量,会对计算结果造成差异,因此需要选择合适过程进行计算;(2)同一条件指测试电流密度、电解液类型、测试温度等外在因素保持一致,选择正负极半电池各自的实际比容量进行计算,避免因上述因素造成容量相差太大,影响N/P比计算。(3)正对面指正负极极片对准的区域。
[说明](1)实验室扣式全电池N/P比计算,一般正极材料组装的半电池取放电比容量,负极材料组装的半电池取充电比容量,以便进行计算;(2)极片打皱、弯曲,可采取减小烘干速率、降低烘干温度或用胶带固定极片,解决方法视具体情况而定。
3.N/P比对电池的影响:(1)N/P比过大即负极过量偏大,虽然能够有效避免析锂,但是正极材料的有效负载量下降,克容量发挥下降,电池能量密度下降;(2)N/P比过小即负极过量偏小,正常循环和电池滥用如过充、过放等情况下析锂风险上升,影响电池性能
3.1.2 Overhang
1.定义:指的是负极相对于正极在长度和宽度方向上多出的部分。主要基于以下考虑:(1)负极的Overhang设计有助于避免在电池充电过程中锂离子在负极表面析出形成锂枝晶,这可以减少锂枝晶穿透隔膜造成内部短路的风险,提高电池的安全性。(2)当负极面积大于正极时,可以确保在电池充放电过程中有足够的空间来接收或释放锂离子,从而保持电池的容量。(3)Overhang设计中负极面积的增加可能会导致电池的首效降低和容量逐渐降低,这是由于部分锂离子会扩散进入负极过量区域,从而会影响电池的电化学性能。(4)Overhang设计虽然可以提高安全性和容量保持,但过量的Overhang会导致电池能量密度降低,因为它们并不贡献于电能存储。
2.设计:在实验室中,对于圆形极片而言,Overhang可认为是面积大小,电池中尺寸大小依据隔膜>负极极片>正极极片的原则进行设计,如直径10mm(或12mm)正极极片,可选用直径12mm(或14mm)负极极片,隔膜选用直径14mm(或16mm、19 mm),避免极片错位导致电池容量衰减快和电池匹配失效,相应尺寸选择视具体情况而定。
3.1.3首次库伦效率(ICE)
1.定义:电池在第一次充放电循环中,放电时释放的电荷量与充电时输入的电荷量之比。首次库伦效率(ICE)反映了电池在首次使用时的能量转换效率。
2.设计:在首次充放电过程中,由于会在材料表面形成SEI膜,导致活性离子减少,从而导致首次充电容量>首次放电容量>后续循环期间放电容量,因此在进行设计时需要注意区别。对于实验室扣式全电池,为避免ICE的影响,一般可以先将正负极分别组装成半电池,循环数圈后再拆开组装全电池,也可以在组装的全电池中加入足量的电解液一定程度上弥补活性离子的损失。
3.预锂化方法:预锂化(Prelithiation)是一种用于提高锂离子电池首次库伦效率和总体性能的技术。它通过在电池制造过程中向电池内部添加额外的锂源,来补偿由于形成固体电解质界面(SEI)层和其他副反应导致的锂离子不可逆损失。以下是一些常见的预锂化方法:(1)化学预锂化。通过化学反应在负极材料表面引入锂源,如使用锂盐溶液与负极材料反应,使锂离子嵌入负极材料中。(2)电化学预锂化。将锂箔、电解液和负极组成系统,通过外加电压使锂离子经过电解液扩散至负极,完成预锂化过程。(3)接触预锂化。在负极材料中掺入金属锂源,利用金属锂与负极材料接触时发生的内短路微腐蚀反应进行预锂化。(4)锂盐辅助预锂化。在电解液中添加特定的锂盐,这些锂盐能够在电池首次充电时分解,释放出额外的锂离子,以补充SEI层形成过程中的锂损失。(5)表面涂层预锂化。在负极材料表面涂覆一层含锂的化合物,如锂的氧化物或锂的金属有机化合物,这些化合物在电池首次充电时分解并释放锂离子。(6)锂合金预锂化。使用锂合金(如锂硅合金、锂锗合金)作为负极材料的一部分,利用合金中的锂在首次充电时提供额外的锂源。(7)喷涂预锂化。将稳定的锂金属颗粒和表面活性剂的混合物喷涂在负极上,形成一层均匀的含锂涂层,以提高电池的寿命周期。(8)机械轧制。通过机械轧制的方式在负极表面引入牺牲锂膜,构建具有不同接触状态的预锂化界面,提高锂的利用率。(9)真空热蒸发。利用真空热蒸发技术在负极表面形成锂薄膜,通过锂蒸汽的高迁移率实现更共形的接触,并具有丰富的电子通道。
[说明]预锂化技术的选择取决于电池的类型、所使用的材料以及制造工艺。通过预锂化,可以提高电池的总容量、能量密度和循环稳定性,从而延长电池的使用寿命。
3.1.4电压范围确定
全电池的电压范围是从正极的最低电压减去负极的最高电压,或者从正极的最高电压减去负极的最低电压。这里取两者中较大的差值来确定全电池的最大电压范围。
计算最大电压范围可用以下方法进行粗略计算:最大电压范围=正极最高电压−负极最低电压。然而,实际应用中,电池的充放电截止电压通常会根据电池设计和安全考虑而有所不同,可能不会使用到整个电压范围,需要根据实际情况进行优化设计。
3.2扣式全电池组装
扣式全电池的组装顺序与半电池组装顺序相类似,不同之处在于若要避免由于形成SEI膜导致库伦效率过低,需对负极进行预锂化处理。在实验室中,可采取将负极材料组装成半电池(也可以将正极材料组装成半电池),进行预循环数圈后拆开,再与正极(或循环后的正极)匹配组装成全电池。以下正负极材料、隔膜、粘结剂和电池壳等请联系新威工作人员。
正极极片制备:将正极材料(如磷酸铁锂、钴酸锂)、导电剂(如Super P、SWCNTs)、粘结剂(PVDF)按照质量比8:1:1(或7:2:1)均匀混合后,加入适量NMP再次均匀混合,涂敷于铝箔上。在鼓风干燥箱烘干至表面无明显溶剂残留,然后转移至真空干燥箱真空干燥。裁切需要的尺寸,即可得到正极极片。
负极极片制备:将负极材料(如石墨、活性炭)、导电剂(如Super P、SWCNTs)、粘结剂(CMC&SBR,1:1)按照质量比7:2:1或8:1:1混合均匀,再加入适量水均匀混合后,涂敷于铜箔上。在室温干燥至表面无明显溶剂残留,然后转移至真空干燥箱真空干燥。裁切需要的尺寸,即可得到负极极片。
[注](1)PVDF可先溶于NMP中配制成一定质量分数的溶液,同样CMC先溶于水中配制成一定质量分数的溶液。
(2)导电剂和粘结剂的选择和占比根据具体材料进行调整。
(3)涂覆完毕后,整块极片是否立马进行烘干,以实际湿度、温度进行调整,上述步骤仅供参考。
组装步骤可参考以下顺序:以CR2032为例,正极壳-垫片(15.6 mm ×0.5 mm)-正极片-电解液-隔膜-电解液-负极片-垫片(15.6 mm ×0.5 mm)-弹片-负极壳,组装顺序和垫片厚度选取视个人习惯而定。
4.扣式全电池实例分析
4.1测试仪器简介
选用新威多通道电池测试系统(如图2所示),进行恒电流充放电测试,以获得正负极材料组装的扣式半电池的实际比容量,再根据上述计算方法对全电池进行设计和组装测试。

图2. 新威电池测试系统
新威多通道电池测试系统还集成了众多工作模式模式:(1)充电模式:恒流充电、恒压充电、恒流恒压充电、恒功率充电;(2)放电模式:恒流放电、恒压放电、恒流恒压放电、恒功率放电、恒阻放电;(3)直流内阻(Direct current internal resistance,DCIR)测试;(4)循环测试;(5)循环嵌套:具有嵌套循环功能,最大支持3层嵌套。更多详细测试功能可咨询新威工作人员。
4.2测试参数设置
测试参数设置选择新威测试仪的恒电流循环模式,倍率可选择倍率模式,参数设置可参考如下设置:对计算好N/P比的正极和负极分别组装成半电池,对半电池在相应的电压范围内以电流密度0.1Ag−1(或更小电流)循环3~5圈后,在手套箱中将半电池各自拆开,取出循环活化后的正负极片,进行全电池组装和后续测试。以磷酸铁锂正极、石墨负极为例,下面截图中的半电池测试电压范围仅供参考,具体电压范围依据具体材料而定。
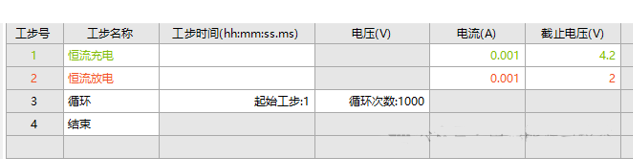
图3. LiFePO4//Li扣式电池循环程序

图4. 石墨//Li扣式电池循环程序
4.3实例分析
以褶皱状C-p-MoS2/CNTs负极材料、Na3V2(PO4)2F3正极材料组装钠离子扣式全电池为例,进行全电池N/P比的计算和电池设计,相关图片和数据来源于SCI论文(1)《Crumpling Carbon-Pillared Atomic-Thin Dichalcogenides and CNTs into Elastic Balls as Superior Anodes for Sodium/Potassium-Ion Batteries》和(2)《On-site conversion reaction enables ion-conducting surface on red phosphorus/carbon anode for durable and fast sodium-ion batteries》。
在这篇文献中,C-p-MoS2/CNTs负极极片的制备是将负极材料、Super P、CMC和SBR按照质量比70:15:15(其中CMC/SBR=1:1),混合后涂覆于铜箔上,经真空干燥后得到极片,极片直径为10mm,负载量为1.2-1.5mg cm−2。组装的钠离子半电池的电压范围为0.01-2.5V(vs.Na+/Na),电解液为1M NaClO4 +EC/PC(1:1, v/v)+5%FEC。相关测试数据如下。
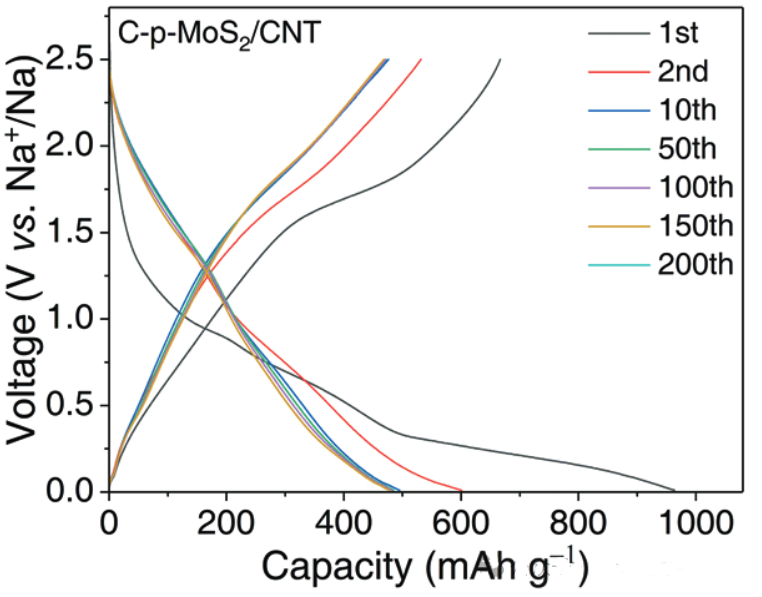
图5. C-p-MoS2/CNTs负极材料前200圈充放电曲线
从图5可知,C-p-MoS2/CNTs负极材料前两圈采用电流密度0.05Ag−1进行循环有利于实现SEI膜的均匀致密形成.该负极材料的首次放电比容量为963mAhg−1,充电比容量为666mAhg−1,首次库伦效率(ICE)为69%.在电流密度0.1Ag−1循环200圈后容量为~460mAhg−1
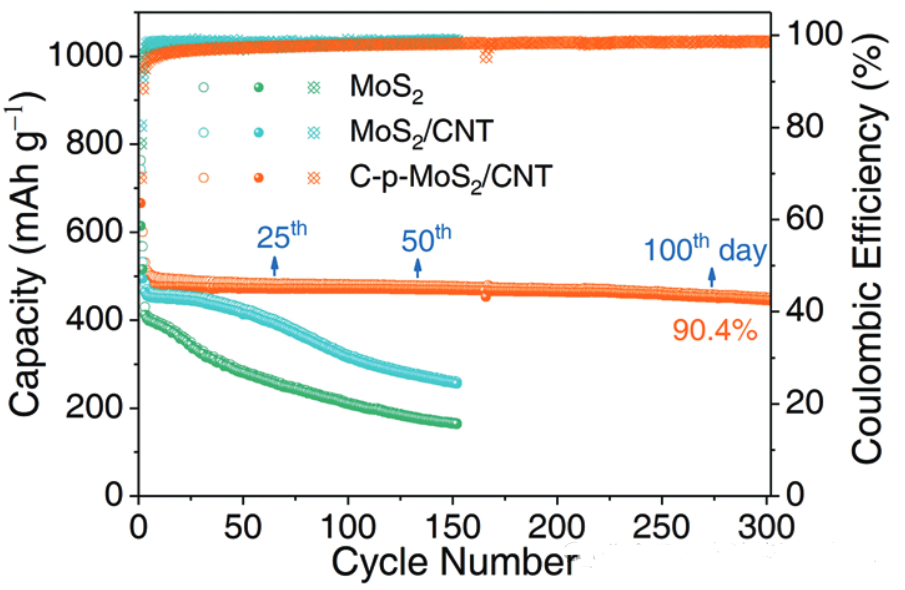
图6. C-p-MoS2/CNTs负极材料在电流密度0.1 A g−1时循环性能图
从图6可知,C-p-MoS2/CNT电极在300个循环后可逆容量达到445mAh g−1,表明该电极材料具有较高的能量存储能力。材料的容量保持率为90.4%,意味着经过多次充放电循环后,电池的容量损失很小,显示出良好的循环稳定性。值得注意的是,这种高容量保持率是在低电流密度(100mAg−1)下进行深度充放电测试的结果,而且测试持续时间超过100天,这表明C-p-MoS2/CNT电极在低充放电速率下具有出色的长期循环性能。
Na3V2(PO4)2F3正极极片的制备是将正极材料、Super P和PVDF按照质量比8:1:1混合后涂敷于铝箔上,真空干燥后得到极片,极片直径为10m,电解液为1M NaClO4+EC/PC(1:1, v/v)+5%FEC,电压范围为2.0-4.5V(vs. Na+/Na)。相关测试数据如下:
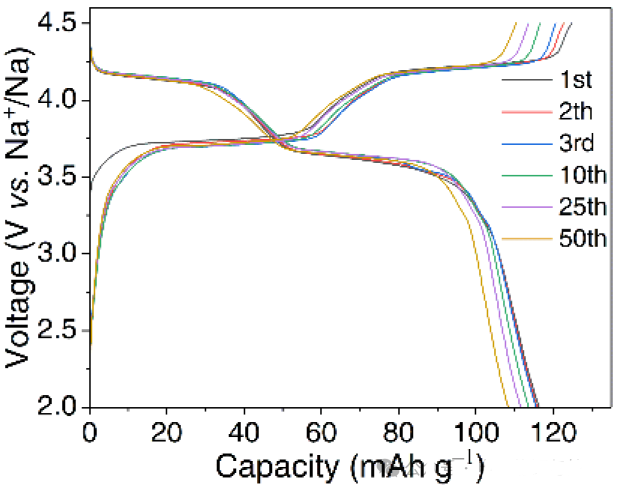
图7. Na3V2(PO4)2F3正极材料前50圈充放电曲线
Na3V2(PO4)2F3正极材料在1C(1C=128mA g−1)首次放电比容量为117mAhg−1,存在两个放电平台(~4.1V和~3.6V)。循环容量的衰减可能来自于高电压循环时电解液溶剂稳定性降低和材料的结构稳定性及产生副反应所导致,可通过碳包覆对正极材料电化学性能进行改善。
依据N/P比计算公式,根据正负极材料的比容量,假定正极极片面积10mm,负载量2.4mgcm−2,容量为117mAhg−1(此处采用1 C容量计算,实际测试时建议采用相同电流密度);负极极片面积12mm,负载量1.2mgcm−2,容量为445mAhg−1(此处采用0.1A g−1循环后容量计算)。因此,N/Pratio=(445×1.2×0.785)/(117×2.4×1)=1.3,式中活性物质占比依据实际计算得到的占比进行计算,此处为了简易计算直接选取活性物质初始占比作为示例。为保证循环的长期稳定性和容量的发挥,该工作中优化后的N/P比为1.2,电压范围为0.6-3.8V。相应组装全电池后的测试数据如图8所示。
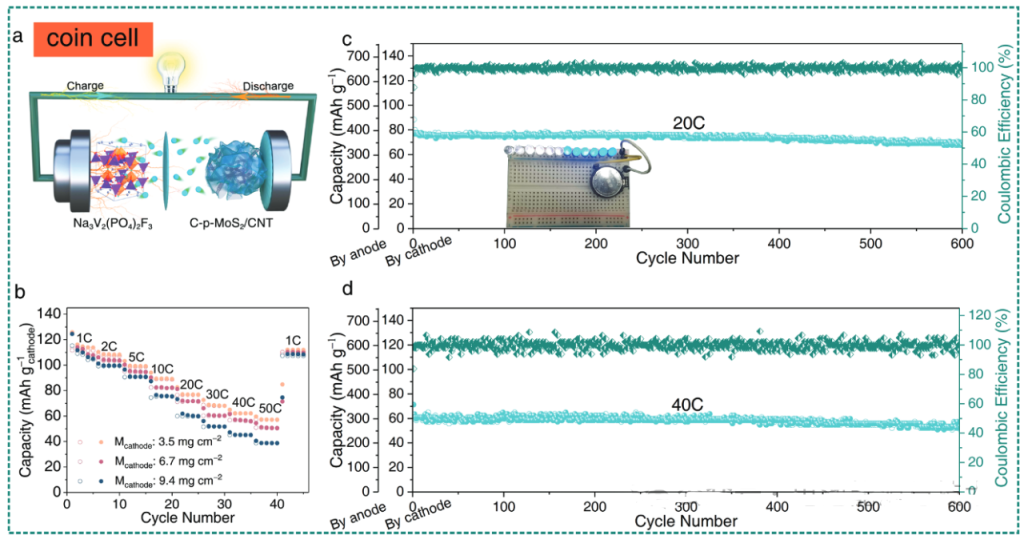
图8. Na3V2(PO4)2F3//C-p-MoS2/CNT钠离子扣式电池电化学性能图
从图8可知,全电池电压范围为0.8-3.6V,在较低负载3.5mgcm−2时,以50C(1C=128mAg−1,基于正极计算)的电流密度获得了高达59mAhg−1(基于正极计算)的可逆容量。当质量负载增加到9.4mgcm−2时,在50C电流密度下仍可提供39mAhg−1的容量,而且在20C的电流密度下经过600个循环后,可保持71mAhg−1的容量,容量保持率为91.5%。即使在40C的高倍率下,经过600个循环后放电容量为52mAhg−1,每圈循环容量衰减率0.021%。
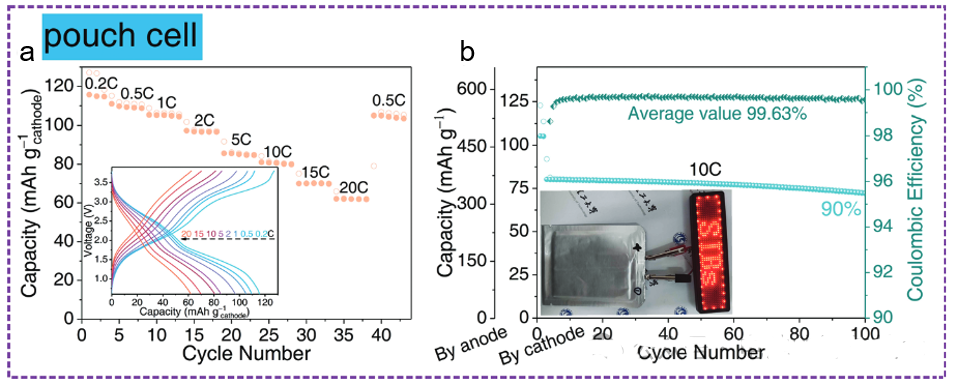
图9. Na3V2(PO4)2F3//C-p-MoS2/CNT钠离子软包电池电化学性能图
采用了尺寸为5.5×4.5cm2的正极、6×5cm2的负极和6.5×5.5cm2的隔膜组装单层软包电池,电化学测试结果如图9所示。软包电池能够在20C的电流密度下提供62mAhg−1正极的相当容量。它还可以在10C的电流密度下循环超过100个周期,并保持其90%的容量,表明Na3V2(PO4)2F3//C-p-MoS2/CNT钠离子软包电池电化学性能优异。
在文献(2)中,负极材料P/C@S负极材料(如图10所示)在电压范围0.01-2.0V内组装成半电池进行了测试,电解液为1M NaClO4+EC/PC(1:1,v/v)+5% FEC。电流密度为0.2Ag−1时具有836mAhg−1的高容量,初始库仑效率(ICE)为74.7%,并且在100个循环后容量保持率为99.3%。电流密度为0.1Ag−1时容量为862mAhg−1。
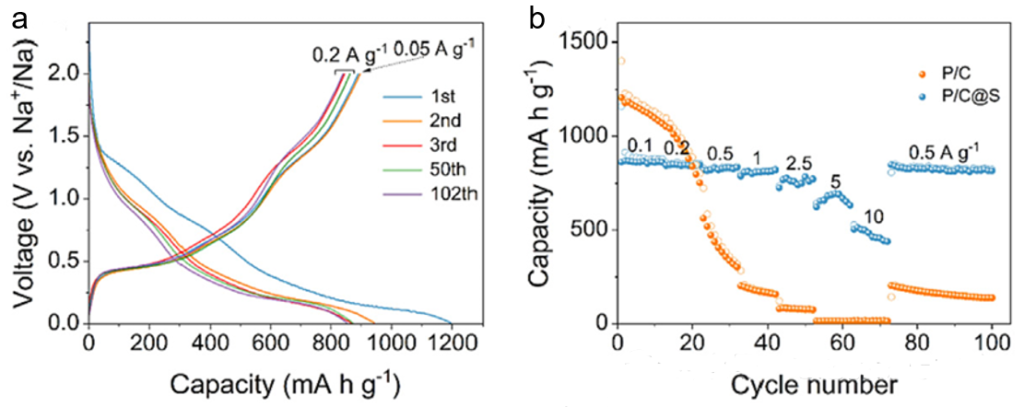
图10. P/C@S负极材料的(a)充放电曲线和(b)倍率性能
Na3V2(PO4)3@C正极材料(如图11所示)在电压范围3.15-3.7V范围内组装成半电池进行了测试,电解液为1M NaClO4+EC/PC(1:1,v/v)+5% FEC。Na3V2(PO4)3@C在1C(1C=110mAg−1)电流密度时容量为~110mAhg−1,首次库伦效率(ICE)为98.5%。在5C循环100圈后容量为~100mAh g−1。
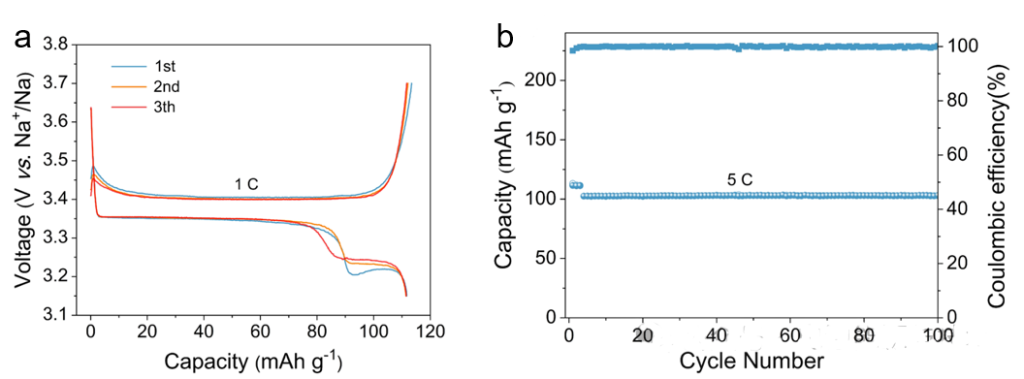
图11. Na3V2(PO4)3@C正极材料的(a)充放电曲线和(b)循环性能。
依据N/P比计算公式,根据正负极材料的比容量,假定正极极片面积10mm,负载量2.4mgcm−2,容量为110 mAh g−1(此处采用1C容量计算,实际测试时建议采用相同电流密度);负极极片面积12mm,负载量1.0mgcm−2,容量为862mAhg−1(此处采用0.1Ag−1循环后容量计算)。因此,N/P ratio=(862×1.0×0.785)/(110×2.4×1) = 2.24,式中活性物质占比依据实际计算得到的占比进行计算,此处为了简易计算直接选取活性物质初始占比作为示例。为保证循环的长期稳定性和容量的发挥,该工作中优化后的N/P比为1.15,电压范围为1.2-3.6 V。相应组装全电池后的测试数据如图12所示。
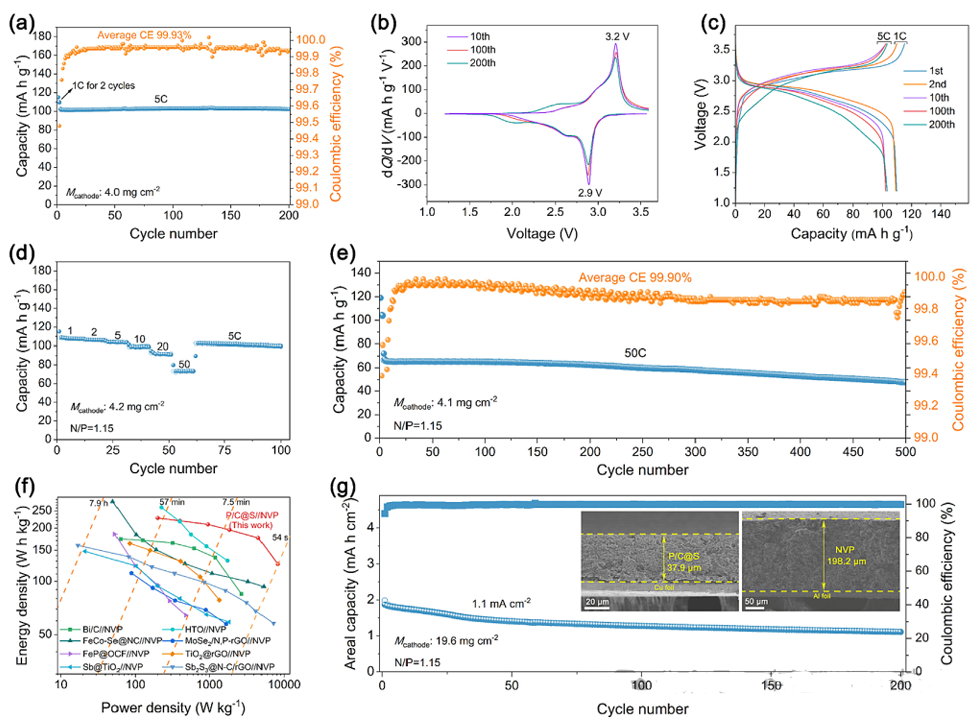
图12. Na3V2(PO4)3@C//P/C@S钠离子扣式全电池电化学性能图
如图12所示,P/C@S||NVP全电池在正极载量约为4mgcm−2的情况下,在5C的电流密度下200个循环后能够实现约103mAg−1的放电容量,平均库仑效率(CE)高达99.93%。同时,全电池电压微分容量(dQ/dV)曲线表明在3.2V和2.9V左右的相对狭窄的阳极和阴极峰,与充放电电压曲线中的电压平台相对应,同时表明全电池平均输出电压~2.9V。全电池在50C电流密度下,它仍能保持1C时容量的67.8%(73mAhg−1)。在50C下500个循环中,容量衰减率仅为每循环0.056%,平均库仑效率高达99.90%。实际的钠离子电池(SIBs)需要在高面容量条件下稳定运行,通过增加活性物质的面载量,这可以最小化集流体、隔膜和电池设备中包装元素的比例,提高能量密度。尽管如此,在全电池中实现具有显著体积效应和不稳定电极/电解液界面的高容量合金型负极材料的高载量是相当具有挑战性的。因此将正极载量增加至19.6mgcm−2、N/P比~1.1的全电池能够实现1.9mAhcm−2的高面容量,同时在1.1mAcm−2下经过200个循环后,可以保持1.1mAhcm−2的面容量。
5.正负极相互关系和全电池应用场景
5.1正负极相互关系
在电池中,正极和负极是构成电池的基本且关键的两个电极,它们相互制约又和平发展,主要包括以下方面:
(1)电化学角色:正极(Cathode):放电时,正极是电子的接收端,发生还原反应;充电时,正极释放电子,发生氧化反应。负极(Anode):放电时,负极是电子的释放端,发生氧化反应;充电时,负极接收电子,发生还原反应。
(2)电势差:电池的电压是由正负极材料的电位差产生的。正极材料通常具有较高的电位,而负极材料具有较低的电位。
(3)能量存储:正负极材料的化学能通过电化学反应转换为电能。电池的总能量与两个电极的容量和电势差有关。
(4)材料选择:正极材料需要具有良好的电化学稳定性和可逆性,如钴酸锂(LiCoO2)、磷酸铁锂(LiFePO4)、锂镍锰钴氧化物(NMC523)等。负极材料需要能够容纳离子的嵌入和脱嵌,常见的有石墨、硅碳、硅氧材料等。
(5)容量平衡:正负极的容量需要平衡,以确保电池在充放电过程中不会因一方容量不足而导致性能降低。
(6)界面稳定性:正负极与电解液之间的界面稳定性对电池性能和寿命至关重要。不稳定的界面可能导致电池性能衰减。
(7)热管理:正负极在充放电过程中会产生热量,需要适当的热管理来防止电池过热
(8)循环寿命:正负极材料的循环稳定性决定了电池的循环寿命。材料的稳定性越高,电池的循环寿命越长。
(9)安全性:正负极材料的选择和设计需要考虑电池的安全性,避免过充、过放、短路等情况下的安全风险。
(10)协同工作:正负极必须协同工作,以实现电池的最佳性能。电池设计时需要考虑电极材料、结构、电解液等的匹配性。
在电池设计和应用中,正负极的关系至关重要,它们共同决定了电池的性能、安全性和寿命。
5.2全电池应用场景
5.2.1扣式全电池应用场景
(1)实验室研究:扣式全电池常用于实验室中评估电池材料的性能,尤其是在研究新材料或改进电池设计时。
(2)性能测试:它们可以用于测试电池在不同条件下的性能,如循环稳定性、倍率性能和电压特性。
(3)教学和培训:在教育环境中,扣式电池可以用来教授电池的工作原理和构造。
(4)小规模设备供电:对于一些小型电子设备,扣式全电池可以作为一个紧凑的能源解决方案。
5.2.2软包电池应用场景
(1)电动汽车(EVs):软包电池由于其高能量密度和设计灵活性,被广泛应用于电动汽车的动力源。
(2)储能系统(ESS):软包电池适用于需要高容量和长寿命的储能系统,如家庭储能、电网调节和可再生能源存储。
(3)便携式电子设备:由于其轻薄的特性,软包电池适用于智能手机、平板电脑和其他便携式设备。
(4)航空航天:在航空航天领域,软包电池可以提供所需的高能量密度和轻量化。
(5)军事和安全:软包电池在军事设备中也有应用,特别是在需要高能量密度和可靠性的场合。
(6)特殊环境应用:软包电池适应性强,可用于深海探索、极地考察等特殊环境。
软包电池由于其形状的灵活性和高能量密度,通常更适合于对空间和重量有特定要求的应用。而扣式全电池则更多地用于研发和教育领域,帮助研究人员和学生更好地理解电池的工作原理和性能表现。
6. 总结
全电池的N/P比是确保电池性能和安全的关键参数。适当的N/P比能够平衡正负极之间的锂离子流量,防止负极过载和析锂现象,从而延长电池寿命并避免安全风险。理想情况下,N/P比应根据电池的应用需求、电极材料特性和成本效益进行优化。经验上,一个较高的N/P比虽然可以提高安全性,但也可能导致材料浪费和成本上升。因此,电池设计中需要通过实验确定最佳的N/P比,以实现性能、安全和经济性的平衡。
通过本文的介绍,相信您已经N/P比的定义和扣式全电池组装、测试参数设置以及数据处理等方面有了一定的了解。在接下来的电化学系列文章中,本团队将为您详细介绍电池主流材料和电池设计相关电化学的测试,欢迎您关注、分享和支持我们的工作。
