浅谈锂钠离子电池枝晶风险程度
一、谁更容易发生枝晶?—“先天”与“现实”的差异
1.从材料本征性质看(先天因素):钠离子电池更容易
①标准电极电位:钠的标准电极电位(-2.71 V vs. SHE)比锂(-3.04 V vs. SHE)高,这意味着钠的热力学还原沉积驱动力比锂小。理论上,钠更难被还原沉积。
②斯托克斯半径和溶剂化能:钠离子半径更大,电荷密度更低,其溶剂化能比锂离子低。这使得钠离子在电解液中更易脱去溶剂壳,界面传输能垒更低,反应动力学更快。
✎关键结论:由于更快的界面动力学和相对“温和”的沉积行为,钠在沉积时形核位点更多,沉积更倾向于呈现苔藓状或颗粒状,而不是尖锐的枝晶。但这并不意味着安全——苔藓状沉积同样会消耗活性物质、导致短路。
2.从实际应用看(现实因素):锂离子电池的枝晶问题更严峻
①能量密度追求:当前锂电池技术正朝着使用锂金属负极的方向发展(如固态电池、锂硫电池、锂空电池),以追求极高的能量密度。而锂金属负极在循环中不可避免地会产生枝晶,这是其最大的技术瓶颈。
②商用负极材料:目前商用锂电多用石墨负极,钠电多用硬碳负极。在快充或低温等极端条件下,锂离子在石墨中嵌入/脱出的动力学较差,容易在石墨表面析出金属锂(析锂),形成枝晶,造成安全隐患。而钠离子在硬碳中的嵌入动力学通常更好,硬碳对钠的析出过电位也更高,相对不易析钠。
③集流体:钠不与铝在低电位下形成合金,因此钠电池正负极都可以使用廉价的铝箔作为集流体。而锂电池的负极必须使用铜箔,因为锂在低电位下会与铝形成合金。铝集流体在一定程度上能更均匀地分布电流,但这不是防止枝晶的主要因素。
总结对比:

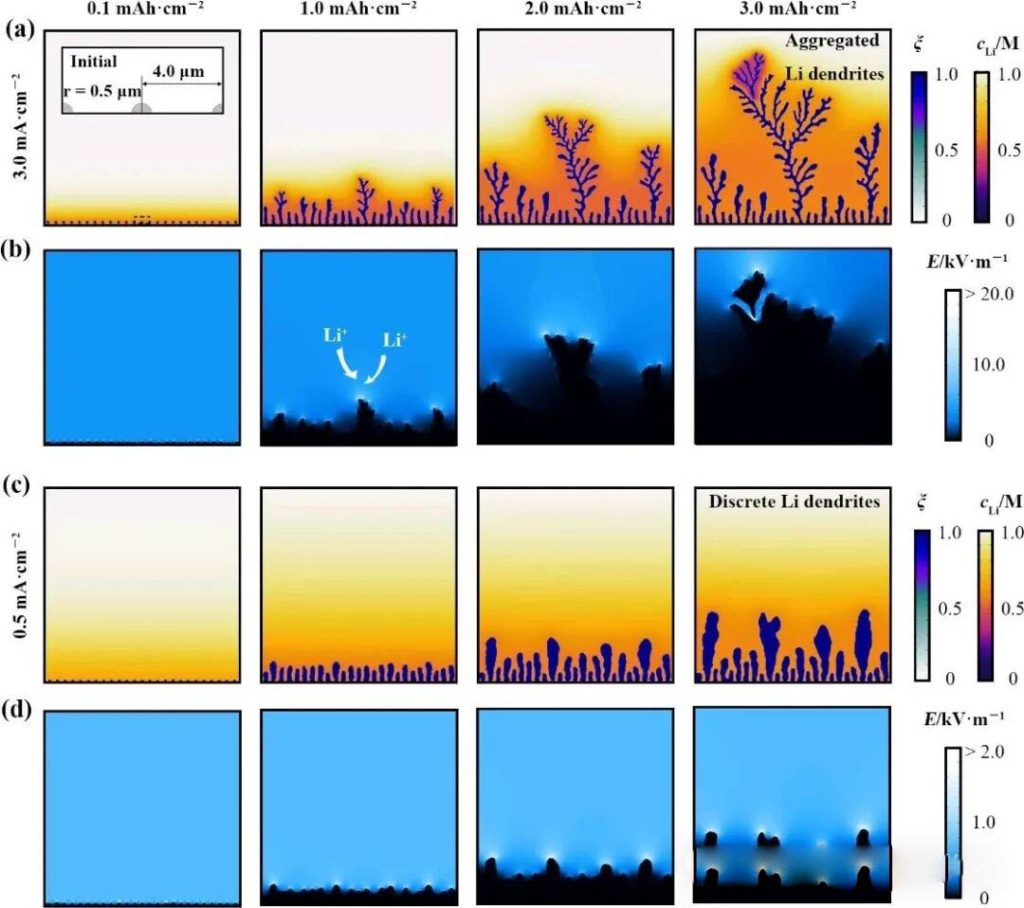
在3.0 mA·cm−2 (a), (b)和0.5 mA·cm−2 (c), (d)条件下,模拟了电沉积过程中(a), (c)锂枝晶的不同形貌演变、锂离子浓度和(b), (d)对应的电场强度。
二、为什么容易发生枝晶?(根本原因)
枝晶的形成是电化学沉积过程中不稳定性的结果,根本原因在于:
1. 不均匀的电极表面:微观上,电极表面存在缺陷、凸起,这些部位电场更强,离子优先在此聚集沉积。
2. 浓度梯度:在放电(沉积)过程中,电极附近的离子被消耗,如果体相扩散速度跟不上,就会形成离子耗尽区(浓度极化)。凸起处扩散路径更短,会优先获得离子补充,从而“疯长”。
3. 固体电解质界面膜(SEI膜):SEI膜的机械强度和化学稳定性至关重要。脆弱的SEI膜会在枝晶生长过程中破裂,新鲜金属暴露形成新的副反应,消耗电解液并加速枝晶生长。
三、如何避免枝晶?
避免枝晶是一个系统工程,核心思路是引导金属均匀沉积/溶解。
1. 电解质工程
①使用高浓度电解液或局部高浓度电解液:增加离子电导,减少浓度极化,并能形成更稳定、更均匀的SEI膜。
②开发新型电解液添加剂:如FEC、VC等,能在电极表面优先还原,形成致密、坚固且离子电导率高的SEI膜,引导离子均匀通过。
③采用固态电解质:这是终极解决方案之一。固态电解质(特别是无机氧化物/硫化物)机械强度高,能物理阻挡枝晶刺穿。但需解决固-固界面接触和离子电导率问题。
2. 负极界面与结构设计
①构建人工SEI膜:在负极表面预先制备一层坚固、离子导电的保护层(如Li3N, LiF等)。
②使用三维多孔负极或复合负极:例如锂/碳复合、锂/合金复合,或者多孔集流体。这可以增加比表面积,降低局部电流密度,提供充足的沉积空间。
③施加外部压力:对于软包电池或实验室研究,施加均匀压力可以改善界面接触,抑制枝晶垂直生长(对固态电池尤其重要)。
3. 电池运营与管理
①优化充电策略:避免大电流(快充)充电,特别是在低温环境下。采用脉冲充电、反向脉冲充电等智能算法,可以“溶解”刚刚萌生的枝晶尖端。
②精确的电池管理系统(BMS):实时监控电池电压、温度和内阻,避免过充和析出。
总之,钠离子电池在材料本征属性上可能比锂离子电池更不易形成尖锐枝晶,但锂电池因能量密度追求而面临的枝晶挑战更为紧迫和严峻。两者都需要通过电解质改性、界面工程和智能管理等多管齐下的策略来抑制枝晶,确保电池安全。
