高温锂电池用混盐电解液体系
不同温度下,电极表面形成的正极电解质相界面CEI膜有所差异,70℃高温对CEI膜的热稳定性要求更加苛刻。本文作者同时使用LiTFSI与LiODFB两种电解液锂盐,在高温70℃下,研究含LiTFSI+LiODFB的酯基电解液与铝箔的相容性;测试采用LiTFSI+LiODFB基电解液的Li/LiCoO2半电池的电化学性能;对循环后的极片形貌进行分析;评估LiTFSI+LiODFB基电解液在70℃下所形成的CEI膜对电池循环性能的影响。
1 实验
1.1 试剂与原料
碳酸乙烯酯EC、碳酸甲乙酯EMC、碳酸二甲酯DMC、LiTFSI、LiODFB、NMP、铝箔、导电炭黑Super P、聚偏氟乙烯PVDF、LiCoO2、锂片、Celgard 2400膜。
1.2 实验仪器
真空干燥箱;电导率仪;电子精密天平;鼓风干燥箱;电池测试系统;实验型辊压机;台式实验涂布机;电化学工作站;震动球磨仪;扫描电子显微镜等。
1.3 电解液的配制
实验在手套箱中进行。将EC、EMC按体积比3∶7加入聚四氟乙烯瓶中配成混合溶剂,再将锂盐LiTFSI和LiODFB按不同物质的量比(见表1)溶解于上述溶液中。配制后封口,静置24h后待用。
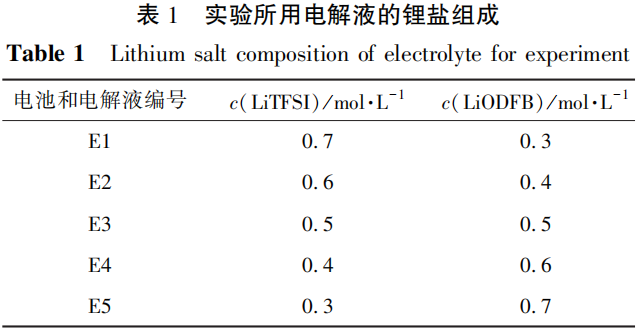
1.4 LiCoO2正极片的制备及扣式电池的组装
将正极活性物质LiCoO2 、Super P和黏结剂PVDF按质量比8∶1∶1置于50mL玛瑙球磨罐中混合,随后加入6mL NMP,以1500r/min转速球磨10min,得到均匀浆料,再涂覆在铝箔上,在120℃下真空干燥12h。自然冷却后,辊压,再裁切成直径12mm的圆片,电子天平称重后,装袋。Al/Li半电池/LiCoO2/Li半电池组装:按正极壳、铝箔(直径12mm)/正极片、电解液、隔膜、锂片、垫片、弹片和负极壳的顺序,组装CR2025扣式电池。静置12h后,进行电化学性能测试。
2 结果与讨论
2.1 Al/Li半电池腐蚀测试
Al/Li半电池在不同电解液中的LSV测试结果见图1。从图1可知,Al/Li半电池在5组电解液中进行LSV测试,电流强度在3.1V处开始增加,对应着LiODFB的氧化分解。
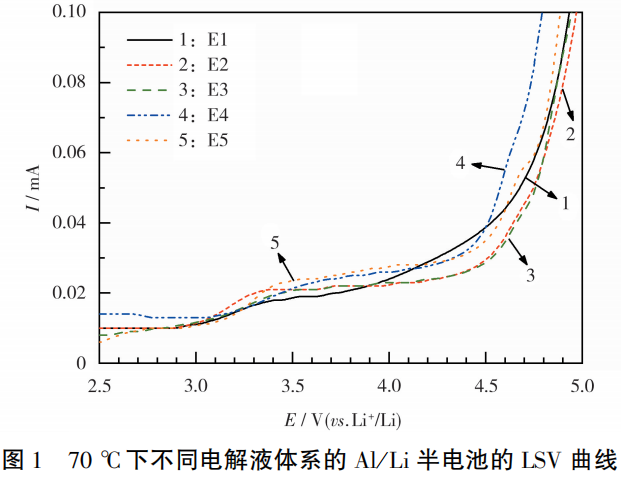
随着LiODFB加入量的增加,各电解液体系的氧化电流强度也随之增强。Al/Li半电池在不同电解液中的CV测试结果见图2。从图2可知,所有电解液的首次循环,在3.1V处均有电流增强的现象,随着循环次数的增加,E1电解液的腐蚀电流进一步增大,而其余电解液的腐蚀电流都趋于稳定。据此认为,E1电解液在70℃下不能完全抑制铝箔腐蚀。 CV测试结果表明,在70℃下,LiODFB的加入,可缓解LiTFSI基电解液对铝箔的腐蚀,但含量要超过0.3mol/L。
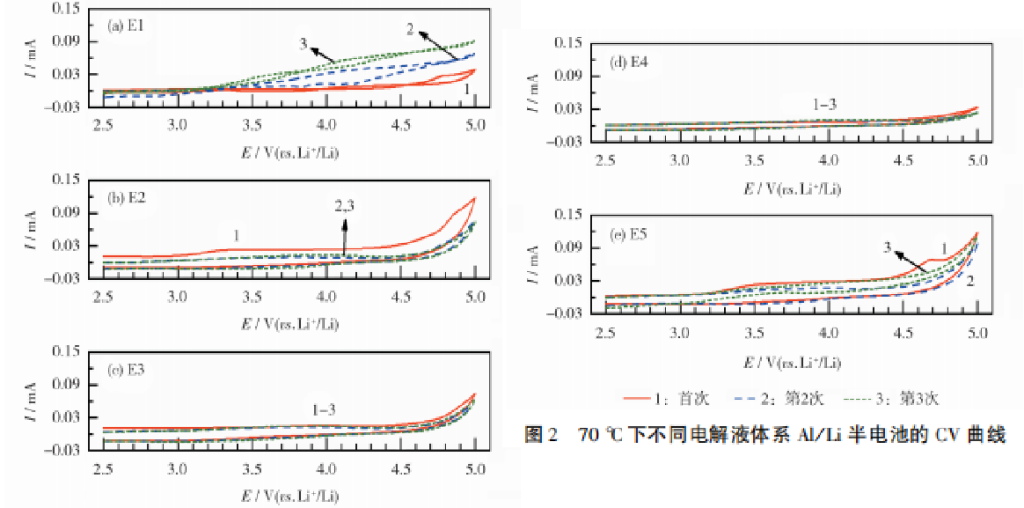
2.2 LiCoO2/Li半电池电化学性能测试
LiCoO2/Li半电池在不同电解液中的循环性能见图3。从图3可知,E1组半电池在70℃下循环60次以后,放电比容量骤然下降,原因在于E1电解液不能完全抑制铝箔腐蚀,导致正极材料从集流体上脱落。
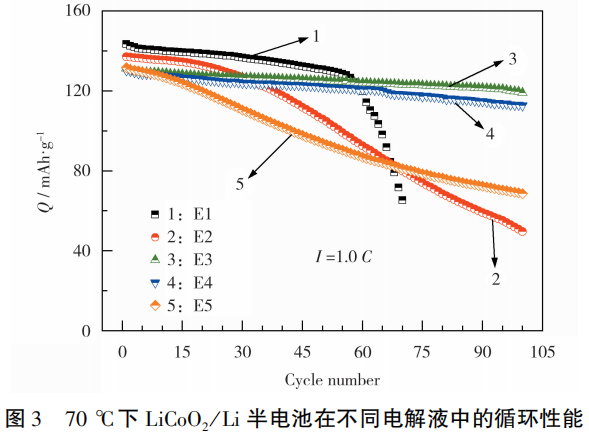
其余4种电解液虽能抑制铝箔的腐蚀,但循环性能差异较大:E3和E4组半电池的首次放电比容量分别为131.2mAh/g、130.3mAh/g,循环100次时的容量保持率依然较高,分别为90.8%、86.5%,原因在于这两种电解液在循环的过程中能在电极表面形成良好的CEI膜,防止电解液进一步分解。
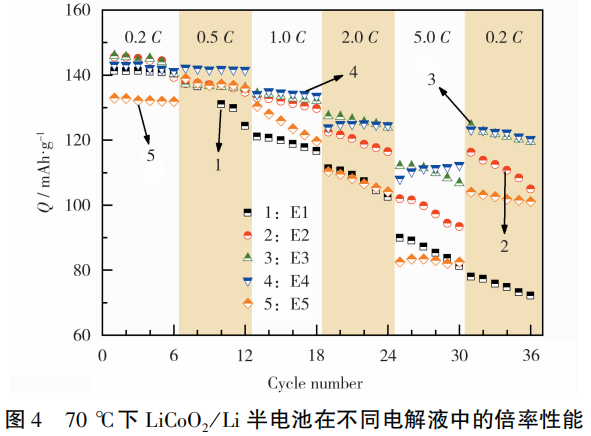
LiCoO2/Li半电池在不同电解液中倍率性能测试结果见图4。从图4 可知,在不同倍率下,E3和E4组半电池的放电比容量要高于其余3种电解液体系的。在经过高倍率的充放电后,E3和E4组半电池的容量衰减也相对较缓。这说明,E3和E4电解液体系在充放电过程中,电极表面形成的CEI膜足够稳定,能抑制高倍率充放电过程的极化现象,减轻不可逆容量损失。
LiCoO2/Li半电池在不同电解液中的CV曲线见图5。不同电解液的离子电导率见图6。从图5可知,每组半电池均有一对氧化还原峰,分别对应于Li+的嵌脱过程。
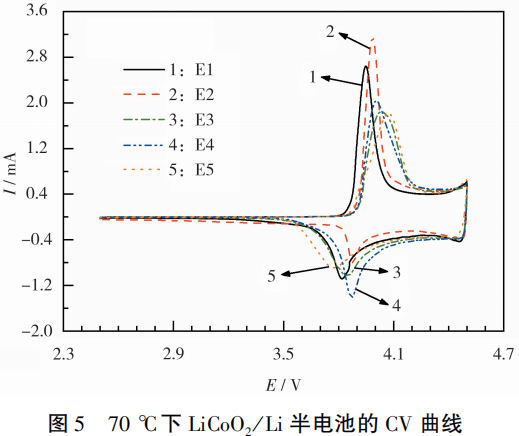
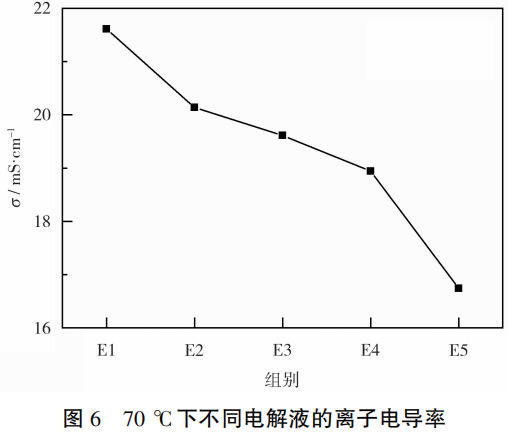
E1和E5组半电池氧化峰和还原峰之间的电势差偏大,表明这两组半电池的极化现象较明显,原因是E1电解液中的LiODFB含量较少,在 70℃ 高温下不能完全抑制铝箔腐蚀,从而导致电池的极化现象加剧。从图6可知,E5电解液中的LiODFB含量过多,导致电解液体系的离子电导率降低,使得电池的极化现象加剧。对比图5中各组半电池的峰电流比可知,E3和E4组半电池的比值最接近1,说明可逆性最好。这也表明,E3和E4电解液可在电极表面形成优异的CEI膜。
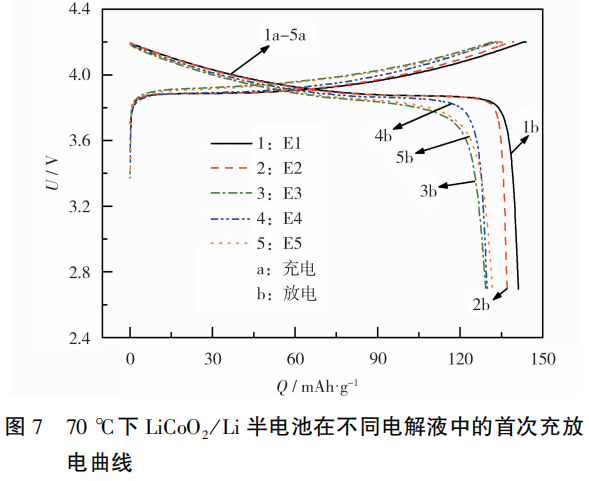
LiCoO2/Li半电池在不同电解液中的首次充放电曲线见图7。由图7数据计算可知,各个电解液体系下的半电池,首次循环的库仑效率均较低,E1~ E5组半电池首次循环的库仑效率分别为98.1%、98.3%、96.9%、97.3%和96.2%,原因在于半电池在首次循环过程中,会消耗一部分的Li+在电极表面形成CEI膜。E1和E2组半电池的放电比容量较高,是因为LiTFSI的含量较高,使得电解液离子电导率增大。
LiCoO2/Li半电池在不同电解液中EIS见图8。从图8( a)可知,随着LiODFB的含量增加,阻抗增大。这是由于LiODFB的加入导致Li+电导率下降,使得电子传输和离子扩散减慢。前25次循环性能测试的结果(图3)也表明,随着LiODFB的含量增加,放电比容量降低,二者可以互相佐证。
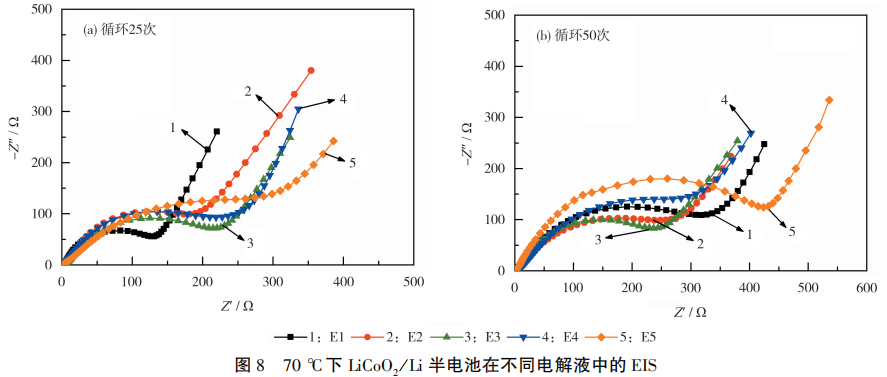
从图8(b)可知,经过50次循环后,5种电解液体系呈现出不同的阻抗变化。E1组半电池内部阻抗急剧增大,是由于LiTFSI对铝箔的腐蚀没有得到抑制。E2组半电池在循环50次后,电池阻抗明显增大,是因为在70℃下,CEI膜中的有机组分会溶解在电解液中,导致CEI膜遭到破环,导致电解液重新与电极界面接触发生副反应。E5组半电池体系在长期循环后,内部阻抗增大,可能是LiODFB的含量过多,降低电解液电导率,导致Li+的反应动力学速率减慢。此外,LiODFB过量时,会在电极界面生成可溶性产物BOF2-,这一类从而使得电池阻抗增大。E3和E4电解液体系循环25次和50次后阻抗变化不大,可认为电极表面形成了均匀的、机械稳定的CEI膜。
LiCoO2/Li半电池在不同电解液中循环后,电极表面的SEM测试结果见图9。E1组半电池在循环的过程中,铝箔被腐蚀,导致电极材料从铝箔上脱落,电池在循环到100次之前就已经失效,而其余4种电解液体系下的半电池均能循环100次。

从图9可知,E2组半电池在循环100次后,电极表面的CEI膜不均匀,是因为LiODFB的含量较少,形成的膜中无机化合物的含量较少,而有机组分较多。在70℃的高温下,CEI膜中的有机组分会重新溶解在电解液中,导致CEI膜被破坏,电池的循环稳定性下降。E5组半电池在循环100次后,电极表面的CEI膜偏厚,是由于LiODFB的过量加入,使得电极表面可溶性产物BOF2-增多,催化电解液溶剂EC的分解,导致电极表面膜层增厚。E3、E4组半电池在循环100次后,电极表面的CEI膜较均匀,且有较高的机械稳定性,使得E3、E4电解液体系的半电池在70℃高温下具有较好的循环稳定性。LiODFB和LiTFSI两种锂盐的协同效应,不仅在电极表面生成了均匀且致密的CEI膜,而且还具有良好的离子电导率。
3 结论
本文作者研究了不同LiODFB/LiTFSI比例的EC+EMC(体积比为3∶7)电解液体系在LiCoO2/ Li半电池中的应用。因为纯LiTFSI会腐蚀铝箔,所以额外加入LiODFB来抑制LiTFSI对铝箔的腐蚀。LiODFB和LiTFSI会在正极表面形成致密且稳定的界面膜,可以提高电池的循环稳定性。结果表明,电解液中LiTFSI的含量为0.7mol/L、LiODFB的含量为0.3mol/L时,所制备的Li/LiCoO2半电池在70℃下会发生铝箔腐蚀现象;而LiODFB的含量大于0.3mol/L时,则能抑制铝箔腐蚀。E3(0.5mol/L LiTFSI+0.5mol/L LiODFB)和E4(0.4mol/L LiTFSI+0.6mol/L LiODFB)组电解液可在电极表面形成良好的CEI膜,在70℃下具有较好的循环稳定性,循环100次后,容量保持率分别为90.8%、86.5%。实验表明,LiTFSI和LiODFB两种盐有较好的协同效应,混合使用时,不仅能够抑制铝箔腐蚀,还具有良好的成膜性和较高的电导率,从而使LiCoO2/Li半电池能够在70℃下稳定循环。
