锂离子电池电压变化内在逻辑
研究电池为什么会有电压,以及电压大小的影响因素的学科叫做电化学热力学。
关键词:
双电层
电极电势
能斯特方程
先看一下下面这三张图,从电子流向、电流流向,电极反应等多个维度去看和思考,真的看懂了你就是高手!
第1张图是电池处于平衡态的开路电压
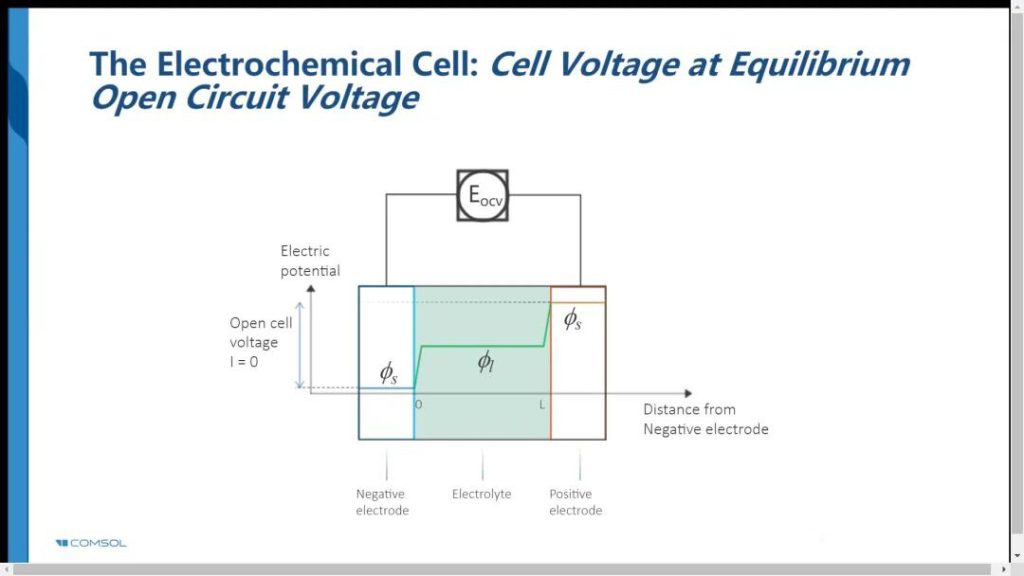
图1的解释:
1.正极带正电,负极带负电,然后与电极接触的电解液就感应出异性电荷,形成双电层,两个双电层的电势差之和就是电池的开路电压。双电层就是个电场,沿着电场线方向电势降低,不信对着图1画一下;
PS:双电层理论不知道的直接百度,这是电化学的源头。
2.溶液不带电,溶液是等势体。
3.电势差都集中在电极表面的双电层中。
第2张图是放电态的电压
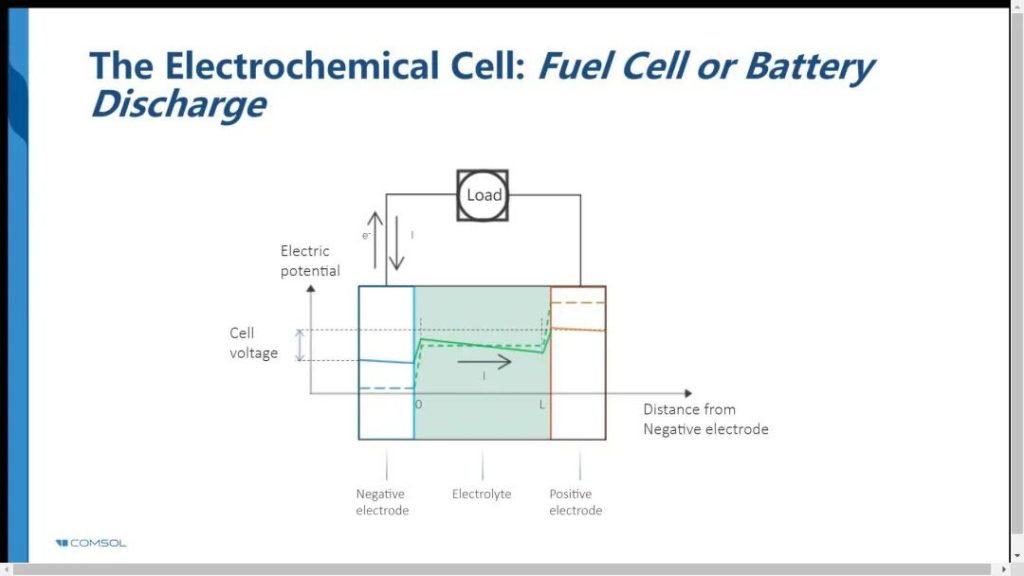
图2的解释:
4.放电时,溶液中的锂离子浓度产生梯度,溶液产生电势梯度,浓度降低的方向就是锂离子(正电荷)移动的方向,也是电势降低的方向。
5.放电时,负极表面锂离子浓度升高,根据能斯特方程:负极发生氧化反应,锂离子是氧化物,氧化物浓度越高,电势越高;
放电时,正极表面锂离子浓度降低,正极发生还原反应,锂离子是氧化物,氧化物浓度越低,电势越低;
不管充电还是放电,无论正极还是负极,锂离子都是氧化物,所以根据能斯特方程,锂离子浓度越高,电势越高,锂离子浓度越低,电势越低。
这与第4点是一致的!
6.电极里面为什么电势会有变化,因为电极是导体或者半导体,有欧姆电阻,沿电流方向电势会有降低。
第3张图是充电态的电压
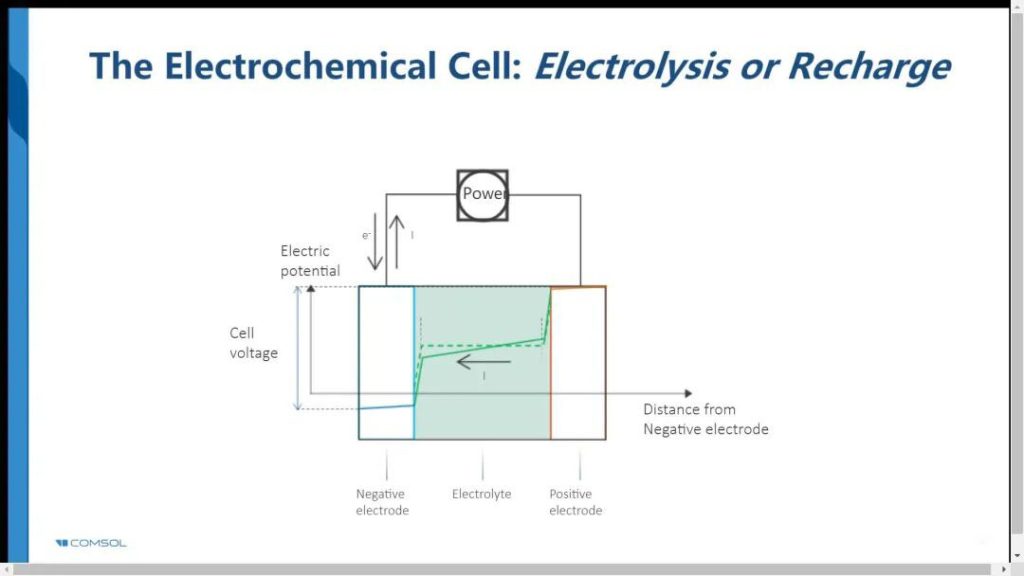
图3的解释:
7.充电时,溶液中的锂离子浓度产生梯度,溶液产生电势梯度,浓度降低的方向就是锂离子(正电荷)移动的方向,也是电势降低的方向。
8.充电时,负极表面锂离子浓度降低,根据能斯特方程:负极发生还原反应,锂离子是氧化物,氧化物浓度越低,电势越低;正极表面锂离子浓度升高,正极发生氧化反应,锂离子是氧化物,氧化物浓度越高,电势越高
不管充电还是放电,无论正极还是负极,锂离子都是氧化物,所以根据能斯特方程,锂离子浓度越高,电势越高,锂离子浓度越低,电势越低。
这与第7点是一致的!
9.能斯特方程
能斯特方程以氧化反应或者还原反应的顺序来写都可以,都是一样的,它是针对单个电极过程而言,结论都是等于平衡电势+(氧化态物质浓度/还原态物质浓度)
或者
平衡电势-(还原态物质浓度/氧化态物质浓度)
PS:如果你要问平衡电势怎么来的?建议百度标准电极电势

