锂离子电池快充电解液设计策略
锂电池的快充性能不论是乘用车还是消费类电池都是目前所追求的性能之一。电池的快充性能与材料,电芯的设计等息息相关。今天我们重点来讨论下电解液端对快充性能的影响。
锂电池中快速充电能力受到石墨负极析锂、层状过渡金属氧化物正极结构稳定性和电解液离子输运速率等因素的限制,而快充时,负极侧的析锂现象被认为是加速容量衰退和增加安全风险的罪魁祸首。在高倍率或低温下充电时,由于过电势较大,使得石墨负极的电位极化到0V(vs.Li/Li+)以下,导致锂金属在石墨表面沉积,引起活性锂损失和内部微短路。
在微观上,充电时锂离子从电解液运输并嵌入石墨的过程分为4步:
(1)溶剂化Li+在电解质中的迁移;
(2)溶剂化Li+到达固体电解质界面(SEI)表面,去溶剂化后进入SEI向石墨迁移;
(3)Li+到达石墨表面发生电荷转移进入石墨内;
(4)Li+在石墨中的扩散。
根据上述4个步骤,将快速充电的限制因素分为两种:一是质量输运,包括Li+在电解质和电极材料中的运输,与步骤(1)和步骤(4)相关;二是电荷转移,涉及Li+的溶剂化/去溶剂化以及Li+在SEI中的扩散,与步骤(2)和步骤(3)相关。就电极而言,确保Li+在负极中的快速扩散和减小负极/电解质界面的运输阻力是实现快速充电的关键挑战。锂离子在电解液中的迁移速度对于电化学动力学至关重要,同时显著影响着锂离子电池的快充能力。促进锂离子在电解液中迁移的方法分为两种:(1)提高离子电导率,(2)提高电解液中的离子迁移数。
接下来我们将从下面几个角度从电解液端优化快充性能
1.促进电解液中锂离子的快速迁移
提高离子电导率
电极反应依赖于电解质在电极之间运输Li+,电解质通过欧姆极化(体电阻Rb和表层电阻Rsl)和电荷转移电阻Rct影响锂离子电池的快充性能。Rb和Rsl的值原则上与电解质的离子电导率相关,而溶剂则在很大程度上决定了液体电解质的离子电导率和工作温度范围。目前商业上常用的电解液溶剂主要是碳酸酯类,包括碳酸乙烯酯(EC)、碳酸甲乙酯(EMC)、碳酸二甲酯(DMC)、碳酸二乙酯(DEC)等。通过溶剂配方的调整能够有效增加电解液的离子电导率,但需要平衡高离子导电性和化学稳定性关系。研究表明,可通过引入具有合适粘度、极性(介电常数)和沸点的助溶剂来改性溶剂共混物,提高电解质离子导电性,合适的助溶剂包括醚类、酯类、和腈类等。
提高锂离子迁移数
在充放电的过程中,阴阳离子在正负极之间进行迁移,所以电解液的电导率由阴阳离子共同组成,高电导率并不一定意味着Li+迁移效率高,在保证高离子电导率的同时,需提高Li+的迁移数。Li+的迁移数定义为Li+的迁移数量占电解液中所有的离子迁移数量的比例。当Li+的迁移数尽可能接近1时,电解液在正负极之间传递电荷效率会显著提高。尽管目前的液体电解质能够在很宽的温度范围内有着很高的电导率且溶解性良好,但实际上Li+的迁移数通常均小于0.5,说明离子电导率实际上大部分是阴离子运动的结果。与阴离子相比,Li+的溶剂化鞘更大,阴离子倾向于向Li+的相反方向迁移,并最终在电极表面积聚,导致一系列的问题:
(1)浓度梯度,限制电池充电或放电的倍率;
(2)浓差过电位,影响电池的工作电压;
(3)限制可使用的电极的厚度。
研究显示,当Li+的迁移数提高到约0.7左右,就能显著提升锂离子电池的快速充电能力,因此在高的电导率下,保持高的迁移系数对于提高锂离子电池的功率密度和能量密度具有重要的意义。
2.降低锂离子去溶剂化能垒
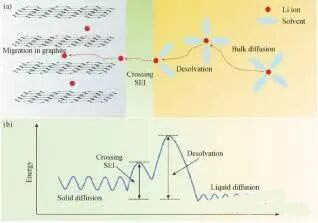
图2 锂离子电池中石墨负极的充电过程示意图以及相应的能量图
图2(a)是锂离子电池在充电过程中Li+的运输示意图,在溶剂化的Li+插入石墨之前,必须剥离它的溶剂化鞘,这一过程称为去溶剂化。在锂离子输运的各过程中,去溶剂化具有最高的能垒(50~70kJ·mol-1)(图2(b)),如果去溶剂化过程不够快,大量的溶剂化Li+到达界面是没有意义的,降低动能势垒加速石墨/电解质界面的去溶剂化过程在快速充电中起着重要作用。
高浓度电解质
由于溶剂和阴离子都可以与锂离子配位,所以实际的溶剂化结构取决于它们之间的竞争位,在稀电解质中,溶剂的数量通常超过阴离子,因此主导了Li+的溶剂化鞘。研究表明,与传统稀释电解质中通常观察到的富含有机化合物(如烷基碳酸锂)的溶剂衍生SEI相比,阴离子衍生SEI富含LiF,能更好地附着在电极表面,形成更薄但更密集的保护层,具有增强的机械性能,能够有效地保护电极免受电解液的进一步分解。更重要的是,阴离子衍生SEI能降低界面电阻实现快速的Li+插层动力学,这是开发快充锂离子电池的关键。为了加速去溶剂化过程,实现阴离子衍生的界面化学,直接的策略是增大阴离子与溶剂的比例,如高浓度电解质(SCE)或局部高浓度电解质(LSCE)。是因为随着盐浓度的增加,阴离子倾向于优先与溶剂分子竞争,形成了新的溶剂化结构,最终改变了界面化学。在高浓度电解质中,所有的阴离子和溶剂与Li+相互作用,形成了与传统电解液完全不同的阴阳离子聚合流体网络结构。由于SCE中缺乏溶剂分子,阴离子必须进入Li+的溶剂化壳层,以满足Li+需要的4~6配位数形成离子-溶剂配位结构。这种独特的结构导致最低未占据分子轨道(LUMO)从溶剂转移到了锂盐,这使得阴离子优先被还原或分解,从而产生稳固的阴离子衍生SEI。
弱溶剂化电解质
降低溶剂化锂离子去溶剂化能垒的另外一个重要方法是调整溶剂的固有溶剂化能力。由于溶剂和阴离子竞相进入Li+的溶剂化鞘,理论上降低溶剂的溶剂化能力可以让更多的阴离子与Li+配合,理想的情况是弱溶剂化电解质(WSE)。与稀电解质相比,WSE的Li+溶剂化鞘中阴离子多,根据计算WSE中的锂离子去溶剂化能垒约为48.2kJ·mol-1,而稀电解液中锂离子被溶剂完全溶剂化,去溶剂化能垒达到54.7kJ·mol-1,这说明Li+溶剂化鞘中含阴离子较多时去溶剂化能垒更低。
总之提高基于锂离子电池的快速充电能力能够加快电动汽车的发展, 虽然仍有许多挑战有待解决,但可以预见的是,开发更多的新型电解液能够获得一些重大突破。
