石墨和钻石,为什么前者被做成电池负极
最近在看到市面上石墨的报价,真是一天不如一天,有位贸易商朋友调侃道:同样都是碳,钻石价格就能够如此稳定,石墨价格却不堪一击,真是同命不同运。突然浮现出几个问题,为什么我们选择石墨作为负极材料,而不是钻石?为什么石墨是黑色,而钻石则是透明?
这几年行业发展得非常迅速,一味的去追求快速的产品输出,直接接受已经成熟的行业体制、设计思维,没有去仔细思考里面的底层逻辑。随着自己重新思考一番,确实还有一些新的收获,古人诚不欺我:温故知新!
1.为什么生活中看到钻石都是小颗粒?
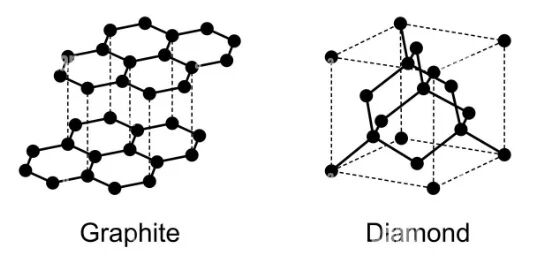
钻石中的碳原子以三维立体结构排列,每个碳原子与周围的4个碳原子通过共价键连接。这些键形成正四面体排列。每个碳原子的1个2s轨道和3个2p轨道发生杂化,形成4个等价的sp³杂化轨道。这些sp³轨道的方向彼此相隔109.5°,形成正四面体。每个sp³轨道与相邻碳原子的sp³轨道重叠,形成强σ键。因此钻石的晶体结构致密,具有极高的硬度。
俗话说过刚则脆,所以我们生活中看到的钻石大部分都是小颗粒的形式存在,直径通常在几毫米甚至更小。大的钻石由于其刚性易碎,随着地质过程(如火山喷发、侵蚀、搬运)可能会破坏原始的大晶体。自然界中大颗粒钻石极为罕见,重量超过1克拉的钻石仅占所有天然钻石的约20%。超过10克拉的钻石更是极其罕见,属于矿物学和收藏领域的珍品。
2.石墨为什么能够成为锂电池负极?
石墨中的碳原子排列成二维层状结构,每一层的碳原子以蜂窝状(六边形)网络排列。每个碳原子与同一平面内的3个碳原子相连,形成共价键,而层间通过较弱的范德华力结合。每个碳原子的1个2s轨道和2个2p轨道发生杂化,形成3个等价的sp²杂化轨道。这3个sp²轨道在同一平面内,彼此间隔120°,与邻近的3个碳原子形成强σ键。剩下的1个未杂化的p轨道垂直于sp²平面,参与形成π键。
π键的作用 未杂化的p轨道与相邻碳原子的p轨道侧向重叠,形成离域的π电子云。这些π电子在整个平面内可以自由移动,赋予石墨良好的导电性。电流是因为电子的定向运动而产生,钻石因为电子都被束缚住,因为钻石是一种很好的绝缘体。
导电性的好坏在选择负极材料的组分时就非常关键,因为锂离子需要接受电子在负极侧还原,构建一个与离子传输速率匹配的导电网络就尤为重要。例如现在非常受到关注的硅,我们知道硅很多都被用于半导体,意味着它的导电能力是远远不如石墨。那么在负极配方设计时,导电剂的比例就应该比石墨体系的更多。
3.钻石为什么是透明的?
那么钻石为什么显示出透明的问题也就很容易回答,单个光子(hv)射入,它并不能激发电子的跃迁或者被吸收,钻石的电子带隙(约5.5eV)很宽,所有的电子都牢牢束缚在共价键中,无法自由移动。大多数可见光的能量不足以激发钻石中的电子,因此光线几乎完全穿过钻石,而不会被吸收或反射,钻石看起来透明。π电子的存在使石墨能够吸收可见光,当光子射入时,自由电子吸收能量后,其运动增强,石墨中自由电子对光子能量的吸收使得其呈现黑色并具有高吸光特性。
4.锂离子电池制造时冷压要注意什么
石墨由于sp2杂化,层内靠共价键存在强度非常高,但层与层之间靠分子间作用力,则极容易发生滑移。在电池负极极片做冷压工序时,石墨的层状结构在受压时容易发生层间滑移,导致颗粒间相对位移,影响极片内部的结构均匀性。在实际操作中,应通过优化压力、速率、配方及设备性能,减少滑移对极片压实质量的影响。同时,通过精确的工艺控制和材料选择,可以在提高压实密度的同时,确保石墨的结构完整性和电池性能的稳定性。
5.钻石是稳定的象征吗?
在室温下,石墨比钻石更加稳定。这是因为石墨的自由能(吉布斯自由能)低于钻石,因此在常压和室温条件下,石墨是碳的热力学稳定相,而钻石是亚稳相。
在标准条件下(298K,1个大气压),石墨的吉布斯自由能比钻石低,约为2.9 kJ/mol。这表明石墨更接近热力学平衡态,具有更高的稳定性。虽然钻石在热力学上倾向于向石墨转变,但这种转变需要克服极高的能垒,因此在室温和常压下,这种转变极其缓慢,几乎可以忽略不计。钻石的sp³杂化结构使得其晶体非常致密,虽然硬度极高,但在热力学上不如石墨稳定。如果钻石是婚姻的象征,那么它本身就是“不稳定”状态。当然,从人类的生命长度来看,能够无限接近于稳定~
