草酸亚铁法为何比固相法更节省锂源
每吨省两万氢氧化锂?草酸亚铁法把水热工艺的”锂浪费”痛点彻底根治
一个痛点:水热法造磷酸铁锂,锂源浪费惊人
先说个行业”潜规则”。
以硫酸亚铁为铁源的传统水热法,制备磷酸铁锂时,锂源(氢氧化锂)的实际用量是理论用量的3倍。
也就是说,每制备1吨纯相磷酸铁锂,需要用到19016mol氢氧化锂,而理论值只需要6339mol。
浪费了多少?66.7%的锂源,直接打水漂。
反应方程式是这样的:FeSO₄+H₃PO₄+3LiOH=LiFePO₄+Li₂SO₄+3H₂O
看出来了没?生成了Li₂SO₄(硫酸锂)这个副产物。
锂源被硫酸根”抢走了”,变成了硫酸锂,没法再用来合成磷酸铁锂。
所以,水热法虽然能制备出颗粒形貌规整、分散性好的磷酸铁锂,但这个”锂浪费”问题,一直是行业痛点。
研究团队,用草酸亚铁替代硫酸亚铁,把这个问题彻底解决了。
核心思路:换个铁源,从化学方程式上根除锂浪费
传统水热法用硫酸亚铁,草酸亚铁法用草酸亚铁。
区别在哪?
反应方程式对比一下:
传统硫酸亚铁法:FeSO₄+H₃PO₄+3LiOH=LiFePO₄+Li₂SO₄+3H₂O
- 锂源用量:3倍理论值(n(Li)实际:n(Li)理论=3:1)
- 副产物:Li₂SO₄(硫酸锂)
草酸亚铁法:FeC₂O₄+H₃PO₄+LiOH=LiFePO₄+H₂C₂O₄+H₂O
- 锂源用量:1倍理论值(化学计量比1:1)
- 副产物:H₂C₂O₄(草酸)
看出来了没?
硫酸亚铁法,因为有SO₄²⁻(硫酸根),会和Li⁺结合生成Li₂SO₄,所以需要过量LiOH来保证反应完全。
草酸亚铁法,草酸根(C₂O₄²⁻)会和H⁺结合生成草酸(H₂C₂O₄),不会”抢”锂。
从化学方程式上,就根除了锂源浪费的根源。
效果有多明显?
制备1吨纯相磷酸铁锂,氢氧化锂用量从19016 mol降到6339 mol。
节省66.7%的锂源。
按照氢氧化锂市场价10万元/吨计算,每吨磷酸铁锂能省下多少钱?
这笔账,我后面算给你看。
工艺详解:190℃最低晶化温度,10小时最佳反应时间
草酸亚铁法不只是省锂,工艺参数也优化到了极致。
1. 最低晶化温度:190℃
研究团队做了温度梯度实验:180℃、190℃、220℃。
180℃:水热晶化24小时,草酸亚铁相的衍射峰仍然很强,说明草酸亚铁没有完全转化为磷酸铁锂。
190℃:草酸亚铁相的衍射峰消失,磷酸铁锂相的衍射峰非常强。
结论:190℃是草酸亚铁水热法制备磷酸铁锂的最低晶化温度。
低于这个温度,反应不完全;高于这个温度,浪费能源。
2. 最佳晶化时间:10小时
固定温度220℃,研究团队做了时间梯度实验:10小时、24小时、57小时。
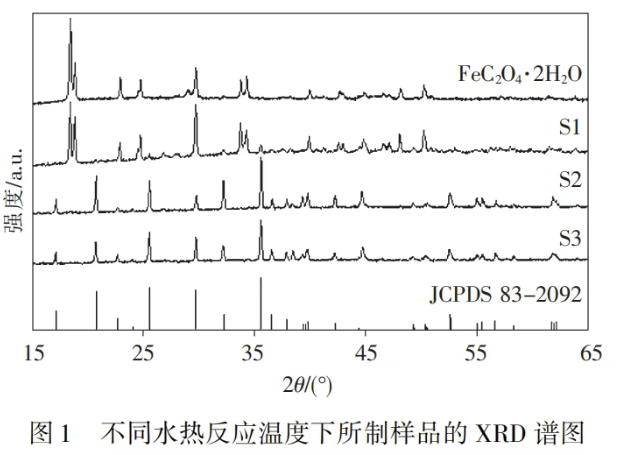
10小时:XRD衍射峰相对强度与标准图谱最为接近。
24小时、57小时:在2θ=38.4°处出现了明显的(002)衍射峰,说明晶体结构发生了变化。
原理:奥氏熟化现象——具有低表面能的大晶体通过消耗较小的晶体而越长越大,具有高表面能的较小晶体由于原子迁移而越来越小直至消失。
结论:10小时是最佳晶化时间。
时间太短,原料转化不完全;时间太长,晶体结构异常,粒径两极分化。
3. 温度上限:280℃时会出现Fe²⁺氧化
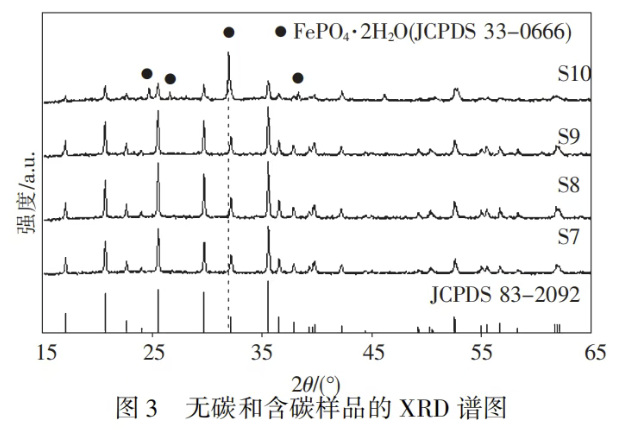
当水热晶化温度达到280℃时,无碳产物中的部分Fe²⁺会被氧化为Fe³⁺,生成FePO₄·2H₂O杂质相。
原理:280℃的晶化温度过高,导致反应釜内空气组分中的O₂活性过高,将Fe²⁺氧化为Fe³⁺。
但添加葡萄糖后,这个问题就解决了。
葡萄糖具有还原性,可以抑制Fe²⁺向Fe³⁺的转化。
4. 最佳工艺窗口总结
无碳磷酸铁锂:
- 晶化温度:240~260℃
- 晶化时间:10小时
碳包覆磷酸铁锂:
- 晶化温度:260~280℃
- 晶化时间:10小时
- 碳源:葡萄糖,添加量6%(质量分数)
- 产物结构:纯相磷酸铁锂,无FePO₄·2H₂O杂质
颗粒形貌:棒状颗粒,分散性好,粒径可控
水热晶化工艺的一个核心优势,就是能减轻产物颗粒团聚。
SEM形貌分析:

S5样品(220℃,10小时):
- 形貌:棒状颗粒
- 尺寸:长2~10μm,宽1~2μm
- 分散性:颗粒较为离散,无严重团聚
S4样品(220℃,57小时):
- 形貌:粒径两极分化
- 小颗粒:长1~4μm
- 大颗粒:棱柱状,长20μm左右
- 原因:晶化时间过长,奥氏熟化现象
G1样品(葡萄糖水热碳化):
- 形貌:球状
- 尺寸:约200 nm
- 用途:作为碳源包覆磷酸铁锂
S7样品(含6%碳包覆):
- 形貌:棒状颗粒
- 尺寸:长1~3μm
- 对比:明显小于S4和S5的颗粒长度
结论:葡萄糖的引入可以降低水热晶化磷酸铁锂产品的粒径。
电化学性能:0.1C放电容量154 mAh/g,理论值96%
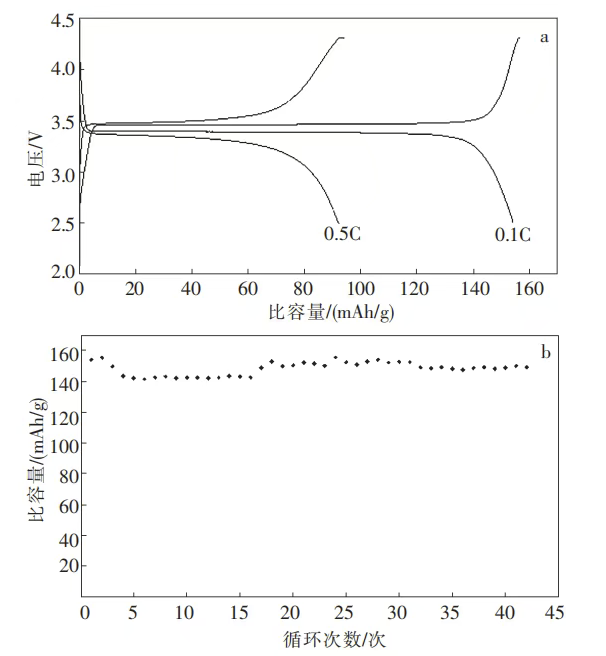
S7样品(草酸亚铁为铁源,260℃晶化10小时,6%碳包覆)的电化学性能测试:
0.1C放电比容量:154mAh/g
- 纯相磷酸铁锂理论最大放电比容量:170mAh/g
- 含6%碳包覆的理论最大放电比容量:160mAh/g
- S7达到理论值的:96.3%
0.5C放电比容量:92mAh/g
循环性能:经过42个循环,0.1C放电容量仍达到149mAh/g
对比传统硫酸亚铁水热法:
- 草酸亚铁法0.1C放电容量更高
- 更适合储能用途的低倍率正极材料
- 但高倍率性能(动力电池)有待提升(可能与水热产品粒径普遍较大有关)
经济账:每吨磷酸铁锂,能省多少锂源?
这才是最关键的。
制备1吨纯相磷酸铁锂:
传统硫酸亚铁水热法:
- 氢氧化锂用量:19016mol
- 质量:19016×41.96(LiOH·H₂O摩尔质量)≈798.6kg
草酸亚铁水热法:
- 氢氧化锂用量:6339mol
- 质量:6339×41.96≈266.2kg
差值:798.6-266.2=532.4kg
节省比例:532.4/798.6=66.7%
成本节省:
- 按氢氧化锂市场价10万元/吨计算
- 每吨磷酸铁锂节省:532.4 kg × 100元/kg = 53240元
- 每吨磷酸铁锂能省5.3万元
这是纯原料成本,还没算上硫酸锂副产物处理成本。
传统工艺生成的Li₂SO₄,要么当废料处理(花钱),要么回收利用(又得建一套装置)。
草酸亚铁法生成的草酸,要么当废料处理(成本远低于硫酸锂),要么回收利用(技术难度低)。
这笔账,草酸亚铁法完胜。
我的观点:草酸亚铁法的”降本+提效”双杀
看完郑州轻工业学院的这项研究,我想说三点。
1. 从”源头控制”比”末端治理”有效
传统水热法的锂浪费问题,行业里试过各种方法优化:
- 改变工艺参数(温度、时间、pH)
- 优化后处理工艺(洗涤、过滤、干燥)
- 回收利用副产物硫酸锂
但这些都是”末端治理”,只能缓解问题。
草酸亚铁法,从源头换了铁源,把问题根除了。
从化学方程式上解决问题,才是最彻底的解决。
2. 190℃最低晶化温度,是工艺优化的”黄金窗口”
研究团队通过系统实验,找到了草酸亚铁法水热合成的最佳工艺窗口:
- 最低晶化温度:190℃
- 最佳晶化时间:10小时
- 最佳温度区间:240~260℃(无碳)/ 260~280℃(含碳)
这些参数,不是拍脑袋出来的,是系统实验的结果。
工艺优化不是”差不多就行”,而是要找到”精确的最佳值”。
3. 5.3万元/吨的降本空间,是企业的”真金白银”
在磷酸铁锂行业,头部企业毛利率已经降到不足5%。
这时候,每吨成本降5.3万元,是什么概念?
这相当于直接提升了10%~15%的毛利率。
在价格战激烈的市场环境下,这样的降本空间,就是企业的生命线。
技术创新,最终要转化为企业的真金白银。
但草酸亚铁法也不是没有挑战:
挑战一:草酸亚铁的成本
草酸亚铁的价格,比硫酸亚铁高。
需要综合计算,锂源节省的钱,能不能覆盖铁源成本增加的钱。
挑战二:草酸的处理
草酸虽然比硫酸锂好处理,但也不是没有成本。
要么当废料处理(需要花钱),要么回收利用(需要建装置)。
挑战三:工艺稳定性
草酸亚铁法虽然是好工艺,但工业化生产时,工艺稳定性是关键。
批次一致性、产品质量稳定性,都需要长期验证。
行业启示:水热工艺的”第二春”
草酸亚铁法这项研究,给行业提了个醒:
水热工艺还有很大的优化空间。
传统水热法因为锂浪费问题,一直没有大规模产业化。
但草酸亚铁法,从化学原理上解决了这个问题。
再加上水热工艺本身的优势(颗粒形貌好、分散性好、批次一致性好),草酸亚铁法很有可能会迎来”第二春”。
未来3~5年,我预计会有更多企业尝试草酸亚铁法,或者开发类似原理的”非硫酸亚铁”水热工艺。
写在最后:从”差不多”到”精确”的技术革命
郑州轻工业学院的这项研究,最打动我的不是5.3万元/吨的降本空间,而是技术研究的”精确性”。
从180℃到190℃,找到最低晶化温度;
从10小时到57小时,找到最佳晶化时间;
从240℃到280℃,找到温度上限;
这些参数,都是系统实验的结果,是精确的数据。
不是”差不多就行”,而是”精确到每一度、每一小时”。
这才是技术创新该有的态度。
草酸亚铁法,不只是省了66.7%的锂源,更是给行业树立了一个榜样:
从”源头控制”解决问题,用”精确数据”验证效果。
核心突破:草酸亚铁替代硫酸亚铁,锂源用量从19016mol降到6339mol(每吨纯相磷酸铁锂),节省66.7%,每吨磷酸铁锂降本5.3万元;190℃最低晶化温度,10小时最佳晶化时间,0.1C放电容量154mAh/g(理论值96.3%)
